11.08.2025
Was Avocados und CED gemeinsam haben
Ultraschallmonitoring bei CED
Symptomfrei ist nicht gleich entzündungsfrei, daher ist es wichtig im Rahmen des CED-Monitorings genauer hinzusehen – der intestinale Ultraschall kann hier eine entscheidende Rolle spielen.
Wer kennt das nicht? Die Avocado im Gemüseregal des Supermarktes wirkt von außen reif und lecker, nach dem Öffnen folgt aber schnell die Enttäuschung: Die Konsistenz ist matschig und die braune Färbung verdeutlicht, dass die Frucht bereits verdorben ist. Dies zeigt, dass sich durch die reine Betrachtung von außen häufig nicht auf den Zustand im Inneren schließen lässt. Bei chronisch-entzündlichen Darmerkrankungen (CED) liegt eine vergleichbare Problematik vor: Nur weil Patient·innen symptomfrei sind, bedeutet dies nicht zwangsläufig, dass das Entzündungsgeschehen im Darmtrakt bzw. in der Darmschleimhaut (Mukosa) abgeebbt ist.
Ein zentrales Therapieziel: Mukosaheilung
Eine Mukosaheilung geht mit zahlreichen Vorteilen für die Patient·innen einher und beeinflusst den Therapieverlauf positiv.
- bessere Langzeit-Outcomes1-3 und vermindertes Krebsrisiko4
- geringes Therapieversagen5,6
- verringerte Hospitalisierung und Verminderung des Operationsrisikos3,5,7
- verminderte Anwendung von Steroiden3,8,9
Daher wird die Mukosaheilung als wichtiges Therapieziel bei CED angesehen10. Sehen Sie sich für weitere Informationen zu diesem Thema gerne das Experteninterview mit dem Gastroenterologen Prof. Dr. med. Dominik Bettenworth an.
Bedeutung eines kontinuierlichen Monitorings
Für das Erreichen eines zentralen Therapieziels der Mukosaheilung ist das Monitoring des Entzündungsgeschehens in der Mukosa von großer Relevanz, um die Therapie gezielt anpassen zu können. Für eine optimale Versorgung der CED-Patient·innen reicht es deshalb nicht aus, nur auf die Symptome und das klinische Ansprechen zu vertrauen. Bedeutsam ist vor allem eine regelmäßige Kontrolle des Krankheitsverlaufs und des Therapieansprechens in der Mukosa. Die STRIDE-II-Konsensusempfehlung rät daher zu einer engmaschigen klinischen Kontrolle der kurz-, mittel- und langfristigen Therapieziele, aber auch zu einer regelmäßigen Überwachung der Mukosaheilung10. Zur Durchführung des Monitorings stehen verschiedene Methoden, z. B. eine für die Patient·innen belastende Endoskopie (Goldstandard), Biomarkeranalysen, aber auch nicht invasive Verfahren wie intestinaler Ultraschall, zur Verfügung10,11.
Nicht invasives Monitoring durch Ultraschall
Die prospektive, nichtinterventionelle Studie TRUST (47 Zentren innerhalb Deutschlands) zeigte, dass die Ergebnisse des intestinalen Ultraschalls gut mit den Ergebnissen der Endoskopie korrelieren und der Ultraschall zum Monitoring des Therapieansprechens bei Morbus Crohn (MC) eingesetzt werden kann. Bereits drei Monate nach Behandlungsbeginn zeigten sich in der Studie signifikante Verbesserungen nahezu aller Ultraschallparameter (p < 0,01), inklusive einer reduzierten Darmwanddicke (BWT, Bowel Wall Thickness), welche wiederum mit einer Reduktion des Entzündungsmarkers C-reaktives Protein (CRP) einherging (p < 0,001)12.
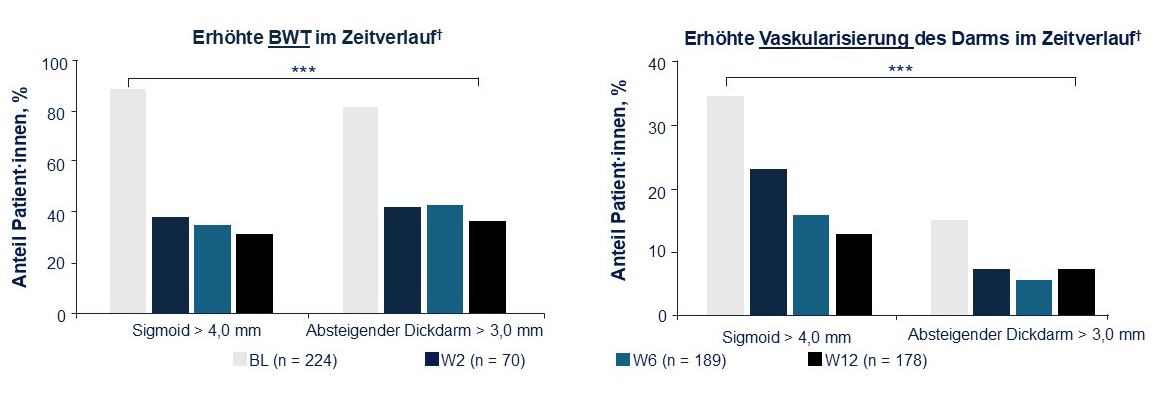
Die prospektive Beobachtungsstudie TRUST&UC (42 Zentren innerhalb Deutschlands) zeigte zudem einen großen Nutzen des intestinalen Ultraschalls bei der Bewertung des kurzfristigen Therapieansprechens bei Colitis ulcerosa (CU). Es wurde deutlich, dass die BWT mit der endoskopischen Krankheitsaktivität korreliert (p = 0,001),*, # was auf das Potenzial des BWT-Monitorings zur Unterstützung der Behandlungsentscheidung hinweist. Des Weiteren zeigte sich, dass ein Ultraschall durch die Visualisierung des Dickdarms zur Quantifizierung von Entzündungen – auch der Mukosa – und krankheitsbedingten Komplikationen eingesetzt werden kann (siehe Abbildung 1)13.
Abbildung 1: Ultraschalluntersuchungen von CU-Patient·innen. Links: Erhöhte BWT im Therapieverlauf. Rechts: Erhöhte Vaskularisierung des Darms im Therapieverlauf.
*** p < 0,001 vs. BL. † Prospektive Beobachtungsstudie, die zwischen November 2015 und März 2018 in 42 auf CED-spezialisierten Zentren in Deutschland durchgeführt wurde, die verschiedene Versorgungsstufen repräsentieren, darunter ambulante und stationäre Versorgungseinrichtungen (45,2 % CED-spezialisierte Praxen, 38,1 % Krankenhäuser und 16,7 % Universitätskliniken). BL: Baseline; BWT: Darmwanddicke (Bowel Wall Thickness); CED: chronisch-entzündliche Darmerkrankung; CU: Colitis ulcerosa; W: Woche. Abbildung modifiziert nach13.
Sie möchten mehr zur Bedeutung des Ultraschalls bei CED erfahren? Einen detaillierten Einblick erhalten Sie in diesem Beitrag.
Vorteile und Einschränkungen des intestinalen Ultraschalls bei CED
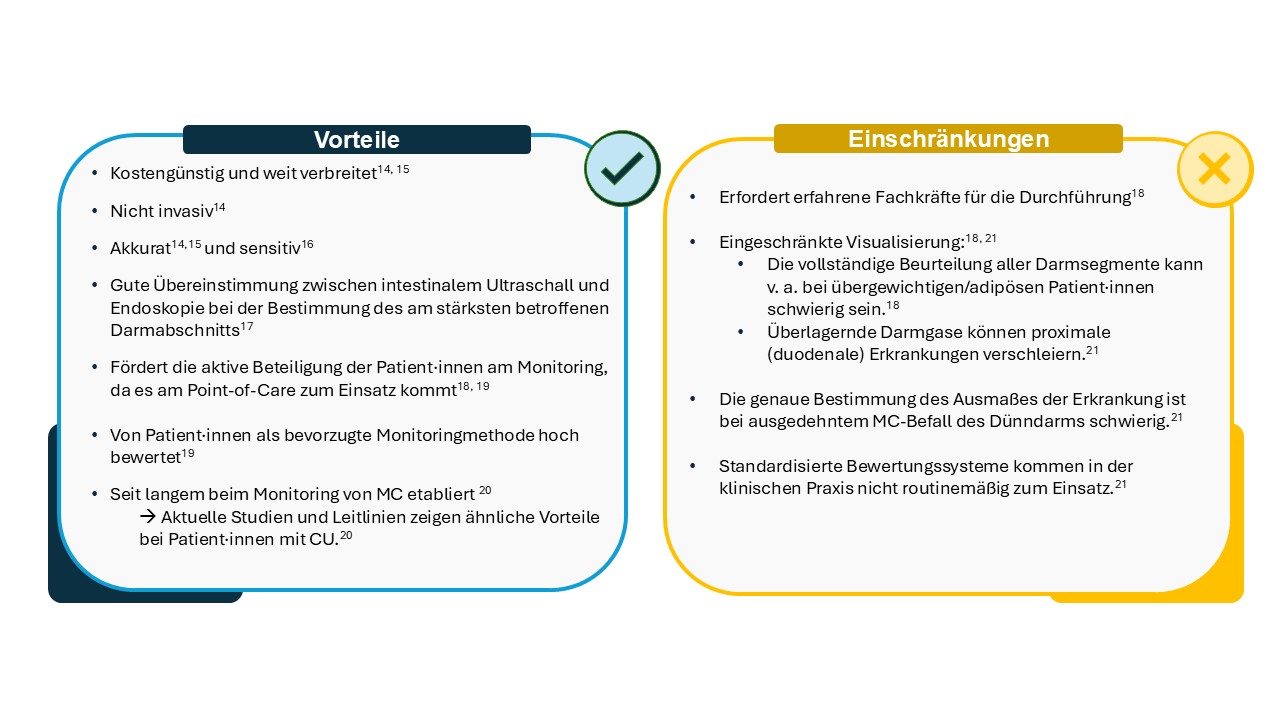
Die Vorteile einer Ultraschalluntersuchung liegen auf der Hand: Die Methode ist nicht invasiv, kostengünstig, patientenfreundlich und dennoch präzise14-16. Der Einsatz ist nicht nur im Rahmen der Diagnostik, sondern auch für das regelmäßige Monitoring der CED-Patient·innen von großem Nutzen17. Dennoch sollten auch die Limitationen des intestinalen Ultraschalls bei CED im Blick behalten werden (siehe Abbildung 2)18,21.
Abbildung 2: Übersicht über die Vorteile und Einschränkungen des intestinalen Ultraschalls bei CED. CED: chronisch-entzündliche Darmerkrankung; CU: Colitis ulcerosa; MC: Morbus Crohn. Abbildung zusammengestellt basierend auf Informationen aus14-21
Insgesamt wird aus der Übersicht deutlich, dass die Vorteile des Einsatzes eines nicht invasiven Ultraschalls im Rahmen des CED-Monitorings überwiegen. Mittlerweile findet der Ultraschall sogar als Endpunkt in klinischen Studien, wie TRUST BEYOND22 und EUROPE (NIS-Studie)23 seine Anwendung.
Fazit
Symptomfreiheit bedeutet nicht automatisch, dass die Patient·innen auch entzündungsfrei sind. Daher ist es wichtig, im Rahmen des CED-Monitorings genauer hinzusehen. Für die Überprüfung des Therapieerfolgs und -verlaufs sowie der Kontrolle zentraler Therapieziele − wie der Mukosaheilung − ist es wichtig, einen klaren Monitoringplan anzustreben. Vor allem das Erreichen der Mukosaheilung ist für das langfristige Therapieergebnis der CED-Patient·innen von großer Relevanz, da hiermit eine Vielzahl positiver Effekte, wie beispielsweise eine Reduktion des Krebsrisikos und eine verminderte Anwendung von Steroiden einhergehen können1-10. Der Einsatz der nicht invasiven Methode des intestinalen Ultraschalls bietet im Rahmen des CED-Monitorings viele Vorteile14-20 und wird bereits als Endpunkt in klinischen Studien eingesetzt22,23.
Funfacts
Es lässt sich nicht immer durch die Betrachtung des Äußeren auf das Innere schließen − das lehrt uns auch die Avocado. Und wer sich trotzdem immer noch fragt, was Avocados nun eigentlich mit Ultraschall zu tun haben: Ultraschall wird zur Extraktion von Avocadoöl sowie zur Bestimmung des Reifegrades einer Avocado eingesetzt24,25.
- Parkes G et al. J Gastroenterol 2023; 58: 990–1002.
- Shah SC et al. Clin Gastroenterol Hepatol 2016; 14: 1245–1255.e1248.
- Rubin DT et al. Am J Gastroenterol 2019; 114: 384–413.
- Korelitz et al. World J Gastroenterol 2014; 20: 4980−4986.
- Yzet C et al. Clin Gastroenterol Hepatol 2020; 18: 2256–2261.
- Yoon H et al. Gastroenterology 2020; 159: 1262–1275.e1267.
- Monstad IL et al. J Crohns Colitis 2021; 15: 969–979.
- Frøslie KF et al. Gastroenterology 2007; 133: 412–422.
- Leung CM et al. J Crohns Colitis 2017; 11: 1440–1448.
- Turner D et al. Gastroenterology 2021; 160: 1570–1583.
- Garcia NM et al. United European Gastroenterology Journal 2022; 10: 1121–1128.
- Kucharzik T et al. Clin Gastroenterol Hepatol 2017; 15: 535–542.e532.
- Maaser C et al. Gut 2020; 69: 1629–1636.
- Maaser C et al. Journal of Crohn's and Colitis 2018; 13: 144–164K.
- Nardone OM et al. Front Med (Lausanne) 2022; 9: 898092.
- Rohatinsky N et al. Crohns Colitis 360 2023; 5: otad012.
- El-Nakeep S. The Egyptian Journal of Internal Medicine 2024; 36: 51.
- Krugliak Cleveland N et al. Current Gastroenterology Reports 2024; 26: 31–40.
- Kucharzik T et al. Clin Gastroenterol Hepatol 2023; 21: 153–163.e112.
- Wilkens R et al. Gastroenterology 2022; 162: 1476–1492.
- Chavannes M et al. Clin Gastroenterol Hepatol 2024; 22: 1790–1795.e1791.
- Kucharzik T et al. Z Gastroenterol 2023; 61: KV059.
- Zeissig S et al. Journal of Crohn's and Colitis 2025; 19: i1647–i1648.
- Pérez-Saucedo MR et al. Food Science and Biotechnology 2021; 30: 1051–1061.
- Fariñas L et al. Journal of Food Engineering 2021; 289: 110266.
* Prospektive Beobachtungsstudie, die zwischen November 2015 und März 2018 in 42 auf CED-spezialisierten Zentren in Deutschland durchgeführt wurde, die verschiedene Versorgungsstufen repräsentieren, darunter ambulante und stationäre Versorgungseinrichtungen (45,2 % CED-spezialisierte Praxen, 38,1 % Krankenhäuser und 16,7 % Universitätskliniken).
# Bei einer Subgruppe von Patient·innen (n = 63, Endoskopie-Datum ± 7 Tage ab dem Datum des Studienbesuchs).
Was Sie sonst noch interessieren könnte:
Sorry, we couldn’t find any articles that match your chosen filters.
Reset filter to see all of our available articles.