03.05.2024
Rundum informiert
Colitis ulcerosa bei Erwachsenen
Der folgende Artikel gibt einen Überblick über die Erkrankung Colitis ulcerosa sowie deren Diagnose und Therapie.
Colitis ulcerosa zählt ebenso wie Morbus Crohn zu den chronisch-entzündlichen Darmerkrankungen (CED). Während die Entzündung bei Colitis ulcerosa zwar in erster Linie auf den Darm – genauer auf die Schleimhaut (Mukosa) und die darunter liegende Bindegewebsschicht (Submukosa) des Dickdarms – beschränkt ist, können auch Beschwerden außerhalb des Verdauungstrakts, sogenannte extraintestinale Manifestationen, auftreten, z. B. an den Gelenken, der Haut, der Leber und den Augen.
Bleibt die Erkrankung unkontrolliert, sind lebensbedrohliche Komplikationen wie das toxische Megakolon (Erweiterung und schwere Entzündung des Darms) möglich und auch das Risiko für Darmkrebs (kolorektales Karzinom) ist bei einer längeren Krankheitsdauer erhöht. Eine frühe Kontrolle des entzündlichen Krankheitsgeschehens ist daher sehr wichtig.
In Deutschland liegt die Prävalenz der Colitis ulcerosa nach Schätzungen bei etwa 470 Betroffenen pro 100.000 Einwohner•innen1,2 und die Inzidenz bei rund vier Neuerkrankungen pro 100.000 Einwohner•innen und Jahr3,4. Männer und Frauen erkranken etwa gleich häufig. Die höchste altersspezifische Inzidenz der Colitis ulcerosa liegt in der Altersgruppe der 16- bis 25-Jährigen4. Bei etwa 20 % aller Patient•innen tritt die Erkrankung vor dem 20. Lebensjahr auf5.
Entstehung und Ursachen der Colitis ulcerosa sind bislang noch nicht vollständig verstanden. Ein Zusammenspiel aus genetischer Veranlagung und Umweltfaktoren, die gemeinsam zu einer fehlerhaften Regulation des Immunsystems des Darms führen, erscheint nach aktuellem Wissensstand plausibel6,7. Bei der Colitis ulcerosa scheinen durch T-Helfer-Zellen vom Typ 2 (Th2-Zellen) vermittelte Immunreaktionen zu überwiegen8,9. Außerdem sind natürliche Killerzellen (NK-Zellen) und Th17-Zellen am Krankheitsgeschehen beteiligt9,10.
Für die Colitis ulcerosa sind nicht nur überschießende Immunreaktionen, sondern auch eine gestörte Barrierefunktion der Zellen, die den Darm auskleiden (Epithelzellen), und ein Verlust der Schleimschicht des Darms typisch. Mikrobielle Antigene können dadurch aus dem Darm in tiefer gelegene Gewebeschichten eindringen und das Immunsystem aktivieren. Es kommt zur Antikörperbildung gegen bakterielle Bestandteile und gegen bestimmte körpereigene Strukturen (z. B. intestinale Becherzellen, Tropomyosin)9,11,12.
Der Zusammenbruch der Darmbarriere führt sekundär zu einer vermehrten Ausschüttung von proinflammatorischen Zytokinen (Eiweiße, die Entzündungsprozesse fördern) wie TNF (Tumornekrosefaktor), Interleukin-1 und Interleukin-1313.
Genetische Risikofaktoren
Wenn ein Familienmitglied an Colitis ulcerosa erkrankt ist, ist das Erkrankungsrisiko bei den Verwandten ersten Grades um das 15-Fache erhöht14. Diese familiäre Häufung lässt auf eine genetische Krankheitskomponente schließen. Tatsächlich sind in der Literatur verschiedene Gene im Zusammenhang mit Colitis ulcerosa beschrieben, die unter anderem bei den folgenden physiologischen Prozessen eine Rolle spielen:
- Funktion und Wiederherstellung der intestinalen Barriere15
- Abwehr mikrobieller Erreger15
- Regulation des angeborenen und des erworbenen Immunsystems15 (z. B. Interleukin-Signalwege oder Differenzierung von T-Helferzellen wie Th1, Th2 und Th1713)
- Bildung von reaktiven Sauerstoffspezies15
- Autophagie (Abbau und Verwertung von Zellbestandteilen im Inneren einer Zelle)15
- Apoptose (programmierter Zelltod)13
- Stress des endoplasmatischen Retikulums15
- metabolische Signalwege, die mit der Zellhomöostase (Gleichgewicht von verschiedenen Zelltypen im menschlichen Körper) assoziiert sind
Einfluss von Umweltfaktoren
Es gibt Hinweise darauf, dass Umwelt- und Lebensstilfaktoren (z. B. Ernährung, Stress) das Risiko beeinflussen, an Colitis ulcerosa zu erkranken13. Die in der westlichen Welt üblichen Hygienestandards werden ebenfalls mit einem erhöhten Erkrankungsrisiko in Verbindung gebracht: Ein seltener Kontakt mit Antigenen (Substanzen, die eine Immunreaktion auslösen können) aus der Umwelt kann möglicherweise die funktionelle Reifung des Immunsystems der Schleimhäute und die Immuntoleranz beeinträchtigen7.
Darüber hinaus sprechen die folgenden Beobachtungen dafür, dass nicht nur die Genetik bei Colitis ulcerosa eine Rolle spielt:
- Stress, negative Lebenserfahrungen, Depressionen13,16 und die Einnahme von nichtsteroidalen Antirheumatika (NSAR)17 tragen unter Umständen zu einer Verschlechterung der Symptome bei.
- Ehemalige Raucher haben ein erhöhtes Risiko, eine Colitis ulcerosa zu entwickeln. Ein schwerer Verlauf der Erkrankung ist bei diesen Patient•innen häufiger als bei Betroffenen, die nie geraucht haben17.
Eine Appendektomie (operative Entfernung des zum Blinddarm gehörenden Wurmfortsatzes) in der Kindheit, die aufgrund einer Blinddarmentzündung durchgeführt wurde, scheint das Erkrankungsrisiko dagegen zu senken17.
Abb. 1: Pathophysiologie von chronisch-entzündlichen Darmerkrankungen. Abbildung modifiziert nach Neurath et al. 201418.
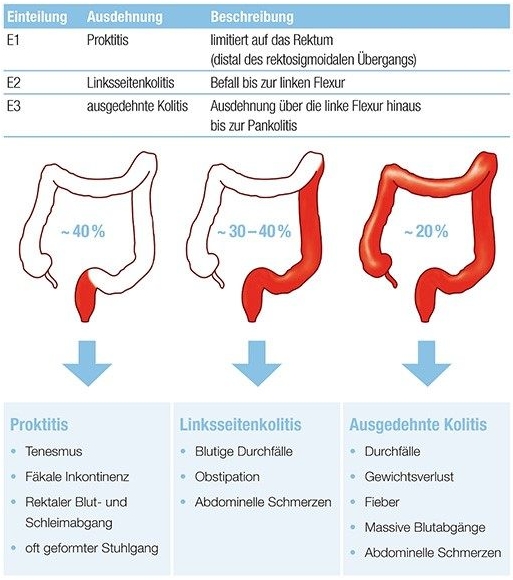
Die Colitis ulcerosa verläuft in der Regel schubförmig: Phasen der Krankheitsaktivität und spontane Phasen der Erholung (Remissionsphasen) mit späteren Krankheitsschüben (Rezidiven) wechseln sich ab13. Im frühen Stadium kann sich die Colitis ulcerosa in Form einer Proktitis (Enddarmentzündung) äußern und im weiteren Verlauf über eine Linksseitencolitis bis zur Pancolitis (Entzündung des gesamten Dickdarms) ausbreiten. Bei einigen Patient•innen liegt bereits zum Zeitpunkt der Diagnose ein fortgeschrittenes Krankheitsstadium vor.
Abb. 2: Ausprägungsformen der Colitis ulcerosa. Abbildung modifiziert nach Silverberg et al. 200519.
Zu den Leitsymptomen zählen blutige und schleimige Durchfälle, kolikartige Bauchschmerzen und Stuhldrang. Darüber hinaus sind Übelkeit, Appetitverlust, Anämie („Blutarmut“), Fieber, Tachykardie (erhöhte Herzfrequenz) und eine allgemein verminderte Leistungsfähigkeit möglich, die auf einen schweren Schub hinweisen können6,20.
Bei 55 % der Patient•innen mit einem starken ersten Schub nimmt die Intensität der folgenden Schübe sukzessive ab21. 45 % der Patient•innen zeigen einen chronischen oder durch wiederkehrende Schübe geprägten Verlauf mit dauerhaftem Therapiebedarf21. Schübe sind per definitionem „häufig“, wenn sie pro Jahr mindestens zweimal auftreten, und „selten“, wenn pro Jahr höchstens ein Schubereignis auftritt6.
Wesentlich für den weiteren Verlauf ist die Krankheitsaktivität in den ersten beiden Jahren nach der Diagnosestellung: Ist diese hoch, steigt das Risiko, dass die Erkrankung auch in den nächsten fünf Jahren aktiv ist, auf 70–80 %6.
Befallsmuster
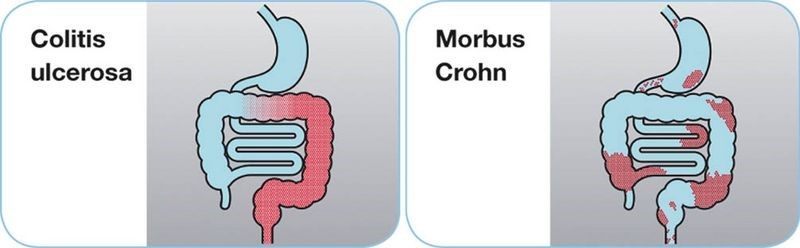
Im Gegensatz zum Morbus Crohn befällt die Colitis ulcerosa zusammenhängende Dickdarmabschnitte und ist auf die Schleimhaut (Mukosa) und auf die darunter liegende Bindegewebsschicht (Submukosa) beschränkt. Je nach Ausdehnung unterscheidet man folgende Befallsmuster:
- Proktitis (Enddarmentzündung, limitiert auf das Rektum; 0–15 cm von der Linea dentata) – das häufigste Befallsmuster7
- Proktosigmoiditis (Entzündung, die auch den Mastdarm und den letzten Teil des Dickdarms, das Sigma, betrifft; 0–35 cm von der Linea dentata)7
- Linksseitencolitis (bis zur linken Flexur)
- ausgedehnte bzw. extensive Colitis (Ausdehnung über die linke Flexur hinaus bis zur Pancolitis [Entzündung des gesamten Dickdarms], Befall des gesamten Kolonrahmens)7,20
Die sogenannte Backwash-Ileitis ist ein Sonderfall, bei dem entzündliche Veränderungen der Mukosa des terminalen Ileums (Krummdarm) auftreten, möglicherweise bedingt durch einen Reflux (Rückfluss) von Darminhalt7. Hier ist eine klare Abgrenzung zwischen Colitis ulcerosa und Morbus Crohn oft schwierig20.
Abb. 3: Befallsmuster bei Colitis ulcerosa und Morbus Crohn. Abbildung modifiziert nach Magro F et al. 20176.
Gastroenterologische Komplikationen
Unkontrollierte Krankheitsverläufe können zu schweren Komplikationen (z. B. zu einem toxischen Megakolon auf dem Boden einer fulminanten Colitis) führen, die ein notfallmäßiges chirurgisches Eingreifen erfordern. Das Darmvolumen ist beim toxischen Megakolon stark erweitert und es besteht die Gefahr einer Darmperforation (Darmdurchbruch). Daher handelt es sich um einen medizinischen Notfall, der einer sofortigen Behandlung bedarf und eine Kolektomie (partielle oder vollständige operative Entfernung des Dickdarms) erfordern kann22.
Auch ein Darmverschluss, der mit schweren Colitis-Verläufen einhergehen kann, muss schnellstmöglich chirurgisch behandelt werden. Schwere Blutungen sind die häufigste Komplikation der Colitis ulcerosa. Sie können unter anderem nach der Entwicklung eines toxischen Megakolons oder nach einer Koloskopie (Darmspiegelung) auftreten.
Extraintestinale Manifestationen
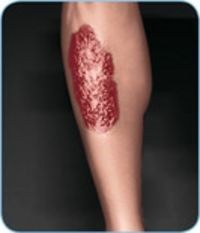
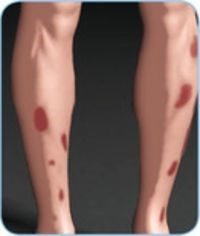
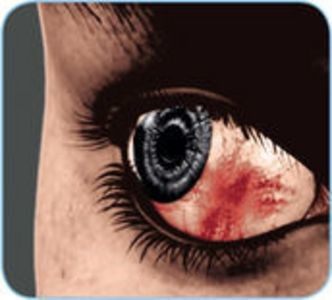
Bei einigen Colitis-ulcerosa-Patient•innen sind neben dem Darm weitere Organe bzw. Organsysteme wie der Bewegungsapparat (hier vor allem die Gelenke), die Augen oder die Haut von der Entzündung betroffen. Einige dieser Erkrankungen werden unter dem Begriff extraintestinale Manifestationen (EIM) zusammengefasst23,24. Dazu zählen z. B. entzündliche Erkrankungen der Haut (Pyoderma gangraenosum, Erythema nodosum) oder der Augen (Episkleritis). Es gibt auch entzündliche Begleiterkrankungen, die zuweilen mit einer Colitis ulcerosa einhergehen, aber nicht als EIM gewertet werden. Dazu zählt z. B. eine rheumatoide Arthritis24.
Wie EIM mit der intestinalen Grunderkrankung konkret zusammenhängen, ist noch nicht eindeutig entschlüsselt. Denkbar ist, dass sich die überschießenden Immunreaktionen im Darm auf weitere Organe ausweiten – z. B. durch den Transport von aktivierten T-Zellen und anderen Entzündungsmediatoren über das Blut. Eine andere Theorie ist, dass EIM von der CED unabhängige Phänomene sind, die auf ein grundlegend verändertes angeborenes Immunsystem und/oder ein gestörtes Darmmikrobiom (Gesamtheit aller Mikroorganismen, die den Darm besiedeln) zurückzuführen sind24.
Eine rasche Remissionsinduktion kann operationspflichtige Komplikationen vermeiden und die Lebensqualität von Colitis-ulcerosa-Patient•innen verbessern. Eine wichtige Voraussetzung dafür ist, dass möglichst früh die richtige Diagnose gestellt wird.
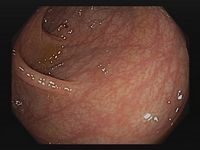
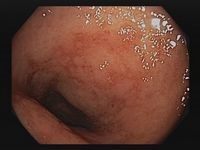
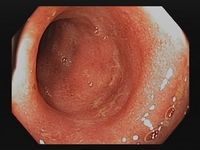
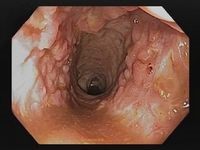
Neben der Befragung der Betroffenen nach ihrer Krankheitsgeschichte (Anamnese), körperlicher Untersuchung, Laborwerten, dem histologischen Befund und dem Ausschluss von enteropathogenen Keimen (Mikroorganismen, die Darmerkrankungen auslösen können) sind verschiedene bildgebende Verfahren (Endoskopie, Magnetresonanztomografie, Ultraschall) für die Diagnosestellung entscheidend. Die differenzialdiagnostische Abgrenzung zum Morbus Crohn kann allerdings mitunter schwierig sein.
Anamnese
Folgende Parameter sollten anamnestisch abgefragt werden:
- Symptombeginn
- Blut/Schleim im Stuhl, Tenesmen (schmerzhafter Stuhldrang), Stuhlinkontinenz
- nächtlicher Durchfall
- Reise- und Ernährungsanamnese
- Darminfektionen
- Medikamenteneinnahme
- Tabakkonsum
- Familienanamnese im Hinblick auf Morbus Crohn und Colitis ulcerosa
- Appendektomiestatus (operative Entfernung des zum Blinddarm gehörenden Wurmfortsatzes)
- Impfstatus
- Allgemeinbefinden
Körperliche Untersuchung
Die körperliche Untersuchung sollte die folgenden Parameter abdecken:
- Puls, Blutdruck (RR), Körpertemperatur, Gewicht, Körpergröße, Body-Mass-Index (BMI), Hinweise auf ungewollten Gewichtsverlust
- abdominelle Druckschmerzen, tastbare Darmschlingen
- Inspektion des Perineums (Gewebebereich zwischen dem Anus und den äußeren Geschlechtsorganen), rektal-digitale Untersuchung
- Prüfung auf extraintestinale Manifestationen (Augen, Haut, Gelenke, Muskulatur, Mund)
Der Nachweis von okkultem Blut (nicht mit dem bloßen Auge sichtbares Blut) im Stuhl erhärtet den Verdacht auf eine CED.
Labor
Im Rahmen der Laboruntersuchung stehen folgende Parameter im Vordergrund:
- großes Blutbild, Blutsenkungsgeschwindigkeit (BSG), C-reaktives Protein (CRP)
- Elektrolyte, Harnstoff, Kreatinin, Leberenzyme, alkalische Phosphatase, Bilirubin, Transferrin, Ferritin
- Urinstatus
- Stuhldiagnostik (pathogene Keime wie C. difficile, Calprotectin)
Bildgebung
Folgende bildgebenden Verfahren können bei Verdacht auf Colitis ulcerosa oder bei Verlaufskontrollen nach bereits gesicherter Diagnose zum Einsatz kommen:
- vollständige Koloskopie (Darmspiegelung) mit Biopsieentnahme17
- bei florider Erkrankung (mit ausgeprägten Symptomen) oft nur Sigmoidoskopie (Spiegelung des Krummdarms) plus Ultraschall der proximalen (zur Körpermitte hin gelegenen) Darmabschnitte17
- Ultraschall zur Erfassung der Ausdehnung und der Aktivität der Entzündung17
- ggf. Magnetresonanztomografie, zum Beispiel zur Differenzialdiagnostik bei nicht eindeutig zu klassifizierender Colitis17
Differenzialdiagnostik
Zum Nachweis einer Colitis ulcerosa müssen alle anderen mit Diarrhö verbundenen Kolonerkrankungen ausgeschlossen werden. Die Abgrenzung zum Morbus Crohn ist häufig schwierig, weshalb die ursprünglich gestellte Diagnose einer CED in manchen Fällen später korrigiert werden muss20.
Bewertung der Krankheitsaktivität
Das Ausmaß der Krankheitsaktivität im Schub, Langzeitkomplikationen und extraintestinale Manifestationen müssen bei der Wahl der Therapie berücksichtigt werden. Nach der Montreal-Klassifikation wird die Krankheitsaktivität der Colitis ulcerosa anhand verschiedener klinischer Parameter in die folgenden vier Stufen unterteilt20:
- Remission (S0): asymptomatische Stühle
- leicht (S1): ≤ 4 Stühle täglich, eventuell blutig; Puls, Körpertemperatur, Hämoglobin und Blutsenkungsgeschwindigkeit (BSG) normal
- mittelschwer (S2): > 4 blutige Stühle täglich ohne oder mit minimalen Zeichen einer systemischen (den gesamten Körper betreffenden) Beteiligung
- schwer (S3): ≥ 6 blutige Stühle täglich und Zeichen einer systemischen Beteiligung, z. B. Körpertemperatur > 37,5 °C, Herzfrequenz > 90 Schläge/min, Hämoglobin < 10,5 g/dl oder BSG > 30 mm in der ersten Stunde.
Eine fulminante Krankheitsaktivität liegt bei einer systemischen Entzündung mit blutigen Durchfällen und starkem Flüssigkeitsverlust, Tachykardie (erhöhte Herzfrequenz), hohem Fieber, Gewichtsabnahme und/oder einem schlechten Allgemeinzustand vor25. Das toxische Megakolon ist eine potenziell lebensbedrohliche Komplikation des fulminanten Schubs. Falls intravenöse Steroide hier keine Symptomkontrolle ermöglichen (steroidrefraktärer fulminanter Schub), sollte eine sofortige operative Versorgung erfolgen17.
Mayo-Score und Montreal-Klassifikation
Während die Montreal-Klassifikation vornehmlich das klinische Bild beschreibt, wird der Mayo-Score vor allem in klinischen Studien verwendet, um die Krankheitsaktivität zu bestimmen. In diesen vierstufigen Index gehen die Stuhlfrequenz, rektale Blutungen, die endoskopische Beurteilung der Mukosa und die Gesamtbeurteilung durch den Arzt bzw. die Ärztin (Physician’s Global Assessment, PGA) ein. Darüber hinaus gibt es noch weitere Scores, die auch ohne koloskopischen Befund anwendbar sind.
Der vollständige Mayo-Score basiert auf einer Skala von 0 bis 12 Punkten. Je höher die Punktzahl, desto höher ist die Krankheitsaktivität.
Interpretation des Mayo-Scores:
- 2–5 Punkte: milde Krankheitsaktivität
- ≥ 6 Punkte: mäßige bis schwere Krankheitsaktivität
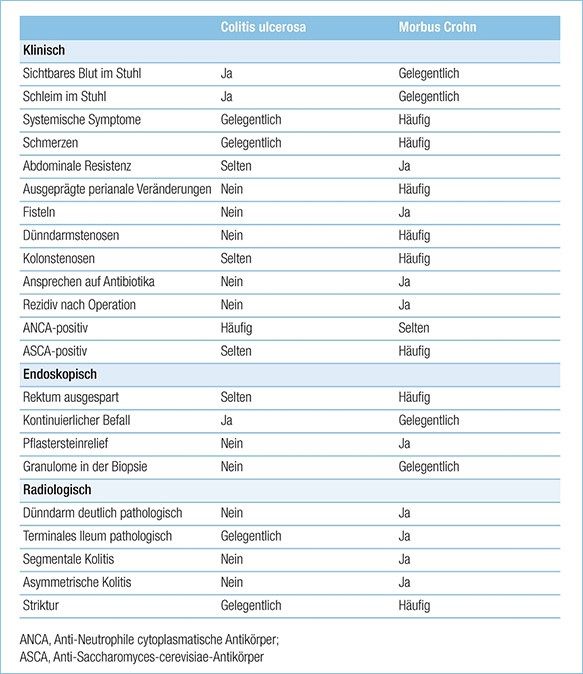
Tab. 1: Unterschiede und Gemeinsamkeiten von Morbus Crohn und Colitis ulcerosa. Aus: Baumgart DC. Diagnostik und Therapie von Morbus Crohn und Colitis ulcerosa. Dtsch Ärztebl Int 2009; 106: 123–13320. Abdruck mit Genehmigung der Deutschen Ärzteverlag GmbH.
Weitere Scores
Der Simple Clinical Colitis Activity Index (SCCAI)26 und der Pediatric Ulcerative Colitis Activity Index (PUCAI)27 können auch ohne koloskopischen Befund angewendet werden.
Fragebogen zur Lebensqualität
Zur Beurteilung der Lebensqualität werden der Inflammatory Bowel Disease Questionnaire (IBDQ) bzw. der Short Inflammatory Bowel Disease Questionnaire (SIBDQ) verwendet28,29.
Das primäre Behandlungsziel bei Colitis ulcerosa ist, rasch eine klinische Remission zu erreichen. Langfristig zielt die Therapie darauf ab, eine steroidfreie klinische und endoskopische Remission im Sinne einer Mukosaheilung (makroskopisch entzündungsfreie Darmschleimhaut) aufrechtzuerhalten. Es gibt zahlreiche Hinweise darauf, dass die Mukosaheilung mit einem günstigen klinischen Ausgang assoziiert ist und einer dauerhaften Schädigung des Darms bzw. CED-assoziierten Operationen vorbeugen kann17.
Bei der Behandlung der Colitis ulcerosa hat sich das sogenannte „Treat-to-Target“-Konzept in der Praxis bewährt. Man versteht darunter eine auf konkrete Ziele ausgerichtete Behandlung mit engmaschigen Verlaufskontrollen, die es bei Bedarf ermöglichen, die Therapie kurzfristig anzupassen und zu optimieren. Auf diese Weise steigt die Chance, dass die ursprünglich gesetzten Therapieziele auch tatsächlich erreicht werden. Idealerweise sollten Ärzt•innen und Patient•innen von Beginn an gemeinsam entscheiden, welche Behandlungsziele ins Auge gefasst werden. Dass die „Treat-to-Target“-Strategie einen hohen Stellenwert hat, betont auch ein internationales Expert•innenkomitee, das im Rahmen der STRIDE-II-Initiative (STRIDE: Selecting Therapeutic Targets in Inflammatory Bowel Disease) definiert hat, welche Ziele bei einer CED-Therapie kurz-, mittel- und langfristig erreicht werden sollen30.
Die medikamentöse Behandlung der Colitis ulcerosa umfasst die Schub- und die Erhaltungstherapie. Während die Schubtherapie dazu dient, akute Symptome zu verringern, zielt die Erhaltungstherapie darauf ab, einen erneuten Krankheitsschub (Rezidiv) zu verhindern3,17,20,31. Vor dem Beginn einer antientzündlichen Therapie sollte eine Entzündungsaktivität objektiv nachgewiesen werden17.
Zur Therapie werden je nach Schwere und Ausdehnung der Erkrankung entzündungshemmende Medikamente nach einem Stufenschema eingesetzt. Falls die Entzündung durch konventionelle medikamentöse Therapiemaßnahmen (Kortikosteroide, Aminosalicylate, Immunsuppressiva) nicht ausreichend beeinflusst werden kann, stehen Biologika, niedermolekulare Wirkstoffe und andere fortgeschrittene Therapien als wirksame Optionen zur Verfügung. Führt die medikamentöse Therapie allein nicht zum Erfolg, kann auch ein chirurgischer Eingriff notwendig sein.
Medikamentöse Therapie
5-Aminosalicylate wirken entzündungshemmend und werden – abhängig davon, wie weit die Entzündung im Dickdarm fortgeschritten ist – lokal oder systemisch bei leichten bis mittelschweren Erkrankungsverläufen eingesetzt 17,20,31.
Derzeit sind Calcineurin-Inhibitoren in Deutschland nicht für die Behandlung der Colitis ulcerosa zugelassen, jedoch empfehlen die Leitlinien ihren Einsatz bei nicht ausreichendem Ansprechen auf eine systemische Steroidtherapie oder bei einer Kontraindikation für Steroide – also wenn bestimmte Umstände vorliegen, unter denen diese Medikamente nicht angewendet werden dürfen. Sobald eine Remission erreicht wurde, sollte eine remissionserhaltende Therapie mit einem Immunsuppressivum oder einem Medikament aus der Gruppe der 5-Aminosalicylate erfolgen17.
Immunsuppressiva wirken entzündungshemmend und werden bei mittelschwerer bis schwerer Ausprägung der Erkrankung angewendet. Da ihre vollständige Wirkung allerdings erst nach zwei bis sechs Monaten einsetzt, ist es oft nötig, die Zeit bis zum Wirkeintritt zusätzlich mit anderen Medikamenten zu überbrücken.
Integrin-Hemmer sind gegen Adhäsionsmoleküle gerichtet, die eine Verbindung zwischen zwei Zellen ermöglichen. Ein Vertreter dieser Wirkstoffklasse ist zur Behandlung der mittelschweren bis schweren aktiven Colitis ulcerosa zugelassen. Der Integrin-Hemmer unterbindet die Entzündungsaktivität im Darm, indem er das α4β7-Integrin blockiert, das bei der Vermittlung von Entzündungsprozessen im Darm eine Rolle spielt.
Die Interleukine IL-12 und IL-23 zählen zu den Schlüsselmolekülen der Entzündungsreaktion bei Colitis ulcerosa. Sie werden unter anderem für die Bildung von Th17-Zellen benötigt und stimulieren auch Zellen des angeborenen Immunsystems32. Die medikamentöse Inhibition dieser Interleukine bietet deshalb einen Ansatzpunkt, um die Entzündungskaskade bei Colitis ulcerosa zu blockieren.
Januskinasen (JAK) sind Enzyme mit einer genregulatorischen Funktion. Sie steuern indirekt die Expression von Genen, die für verschiedene Entzündungsmediatoren kodieren und die bei der Pathogenese der Colitis ulcerosa eine wichtige Rolle spielen32. JAK-Inhibitoren ermöglichen es daher, mehrere Signalwege, die durch JAK gesteuert werden und Entzündungen im Körper fördern, mit nur einem Medikament abzuschwächen. Wie Biologika können auch JAK-Inhibitoren unter anderem im Rahmen der Remissionserhaltung oder bei steroidabhängigen/refraktären Verläufen zum Einsatz kommen – zum Beispiel, wenn Patient•innen auf eine konventionelle Therapie nicht oder nur unzureichend ansprechen oder diese nicht vertragen.
Kortikosteroide haben eine stark entzündungshemmende Wirkung und wirken schnell. Sie werden im akuten Entzündungsschub angewendet – sowohl bei geringer, mittlerer als auch schwerer Krankheitsaktivität. Kortikosteroide sollten jedoch nicht langfristig eingenommen werden, da eine dauerhafte Einnahme zu teils schweren Nebenwirkungen führen kann33.
Das Molekül Sphingosin-1-Phosphat (S1P) ist mit ausschlaggebend dafür, dass aktivierte T-Zellen die Lymphknoten verlassen und in entzündetes Gewebe einwandern. Wird diese Signalkette durch einen S1P-Rezeptormodulator unterbunden, verbleiben die Lymphozyten in den Lymphknoten. Dadurch wird das adaptive Immunsystem gebremst32.
TNFα ist ein Entzündungsmediator, der unter anderem den NF-κB-Signalweg aktiviert und somit zur Sekretion von verschiedenen Zytokinen beiträgt34. TNF-Antagonisten kommen bei mittelschweren bis schweren Krankheitsverläufen zum Einsatz, wenn Patient•innen auf konventionelle Therapien (z. B. Kortikosteroide und Immunsuppressiva) nicht ausreichend angesprochen haben. Die Therapieoption besteht auch dann, wenn konventionelle Therapien kontraindiziert sind oder die Patient•innen diese nicht vertragen. Wenn mit TNF-Antagonisten eine Symptomverbesserung erreicht wird, können diese Medikamente auch als Erhaltungstherapie weiter verabreicht werden.
Nichtmedikamentöse Konzepte
Bei Patient•innen, bei denen die medikamentöse Therapie nicht zum gewünschten Therapieziel führt oder bei denen es zu Komplikationen kommt, sollte eine Operation in Betracht gezogen werden17. Dabei wird entweder ein künstlicher Darmausgang (Stoma) gelegt oder aus Teilen des Dünndarms ein künstlicher Enddarm gebildet und mit dem verbliebenen natürlichen Darmausgang verbunden (Pouch). Die Pouchoperation erzielt für Patient•innen eine bestmögliche Lebensqualität mit durchschnittlich fünf bis sechs Stuhlgängen pro Tag und mit dem Erhalt der Kontinenz bei über 90 % der operierten Patient•innen17.
Krebsprophylaxe durch wirksame Therapie
Eine frühzeitig eingeleitete Therapie der Colitis ulcerosa ist auch wichtig, um das Risiko für kolorektale Karzinome zu verringern. Da mit einer Colitis ulcerosa – abhängig von der Ausdehnung und der Dauer der Erkrankung – ein erhöhtes kolorektales Karzinomrisiko einhergeht, empfiehlt die S3-Leitlinie der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten (DGVS)17 bei linksseitigem oder distalem (weiter weg von der Körpermitte gelegenen) Befall ab dem achten Erkrankungsjahr eine Koloskopie in ein- bis vierjährlichen Intervallen. Bei einer primär sklerosierenden Cholangitis ist das Karzinomrisiko zusätzlich erhöht. Daher sollten die Vorsorgekoloskopien in dieser Konstellation jährlich erfolgen17,20.
- Mueller S et al. Journal of Crohn's and Colitis 2021; 15: S587-S588.
- Hein R et al. Scand J Gastroenterol 2014; 49: 1325-1335.
- Kucharzik T et al. Dtsch Arztebl Int 2020; 117: 564-574.
- Ott C et al. Eur J Gastroenterol Hepatol 2008; 20: 917-923.
- Sinha C et al. Crohn’s Disease. In.; 2010: 193-199.
- Magro F et al. J Crohns Colitis 2017; 11: 649-670.
- Harrisons Gastroenterologie und Hepatologie, 1. Auflage; Martin Zeitz, Hartmut H.-J. Schmidt, Christian Bojarski (Hrsg.); ABW Wissenschaftsverlag, 2011.
- Heller F et al. Gastroenterology 2005; 129: 550-564.
- Neurath MF. Nat Immunol 2019; 20: 970-979.
- Fuss IJ et al. J Clin Invest 2004; 113: 1490-1497.
- Homsak E et al. Wien Klin Wochenschr 2010; 122 Suppl 2: 19-25.
- Geng X et al. Gastroenterology 1998; 114: 912-922.
- Danese S et al. N Engl J Med 2011; 365: 1713-1725.
- Vermeire S. Aliment Pharmacol Ther 2006; 24 Suppl 3: 2-10.
- Khor B et al. Nature 2011; 474: 307-317.
- Baumgart DC et al. Lancet 2007; 369: 1627-1640.
- Kucharzik T et al. Z Gastroenterol 2023; 61: 1046-1134.
- Neurath MF. Nature Reviews Immunology 2014; 14: 329-342.
- Silverberg MS et al. Can J Gastroenterol 2005; 19 Suppl A: 5a-36a.
- Baumgart DC. Dtsch Arztebl International 2009; 106: 123-133.
- Solberg IC et al. Scand J Gastroenterol 2009; 44: 431-440.
- Desai J et al. Clin Exp Gastroenterol 2020; 13: 203-210.
- Levine JS et al. Gastroenterol Hepatol (N Y) 2011; 7: 235-241.
- Greuter T et al. Gut 2021; 70: 796-802.
- Albert J und Fleig W. Ort der Entzündung im Darm bestimmt Behandlungskonzept. Ärztezeitung; veröffentlicht am 02.11.2005; verfügbar unter https://www.aerztezeitung.de/Medizin/Ort-der-Entzuendung-im-Darm-bestimmtBehandlungskonzept-377405.html.
- Walmsley RS et al. Gut 1998; 43: 29-32.
- Turner D et al. Gastroenterology 2007; 133: 423-432.
- Irvine EJ et al. Am J Gastroenterol 1996; 91: 1571-1578.
- Jowett SL et al. Am J Gastroenterol 2001; 96: 2921-2928.
- Turner D et al. Gastroenterology 2021; 160: 1570-1583.
- Harbord M et al. J Crohns Colitis 2017; 11: 769-784.
- Cohen NA et al. Curr Opin Gastroenterol 2021; 37: 357-363.
- Bruscoli S et al. Front Immunol 2021; 12: 691480.
- Billmeier U et al. World J Gastroenterol 2016; 22: 9300-9313.
Was Sie sonst noch interessieren könnte:
Sorry, we couldn’t find any articles that match your chosen filters.
Reset filter to see all of our available articles.