Leucemia Linfatica Cronica
Informazioni sulla patologia
È la forma più comune di leucemia negli adulti nei paesi occidentali e si caratterizza per un accumulo progressivo di linfociti B anormali nel sangue, nel midollo osseo e nei linfonodi.
Obiettivi terapeutici
La Leucemia Linfatica Cronica (LLC) è un tumore maligno linfoide caratterizzato dalla proliferazione incontrollata dei linfociti B CD5+ maturi nel sangue, nel midollo osseo e nel tessuto linfoide.1
La malattia può avere un decorso stabile, ma può anche diventare aggressiva e presentare ricadute frequenti oppure trasformarsi in un linfoma aggressivo, tipicamente linfoma diffuso a grandi cellule B (DLBCL) mediante la trasformazione di Richter.1
Nella maggior parte dei casi la LLC resta una malattia incurabile. L’obiettivo della terapia è quello di migliorare la qualità della vita e prolungare la sopravvivenza. La sopravvivenza dipende solitamente dagli effetti della terapia e dalla sequenza di trattamento somministrata durante il decorso della malattia.2
Terapie della LLC
Il trattamento della LLC si è modificato in modo importante negli ultimi anni.1 La terapia standard in precedenza era basata su agenti chemioterapici in monoterapia o in combinazione con anticorpi monoclonali anti-CD20.1 La proteina CD20 è espressa sulla superficie della maggior parte delle cellule B trasformate e l’introduzione del primo anticorpo monoclonale anti-CD20 nel 1998 ha migliorato il trattamento dei linfomi non-Hodgkin CD20 positive, compresa la LLC.3
Oggi, la chemioimmunoterapia a tempo limitato dovrebbe essere considerata solo per i pazienti con un profilo mutazionale favorevole, cariotipo non complesso, e solo se le target therapy non sono rimborsate.4
Nel caso di scelta della chemioimmunoterapia è fortemente raccomandato di informare e parlare con il paziente delle probabili tossicità a breve e lungo termine, includendo informazioni relativamente al rischio di sviluppare neoplasie mieloidi.4 Le target therapy dovrebbero essere sempre la prima scelta.4
Target Therapy
Le target therapy rappresentano una potente strategia contro la LLC3 e hanno rivoluzionato la terapia di prima linea di questa malattia.1,3,5
Lo standard of care nella gestione della LLC è passato dalla chemioimmunoterapia a terapie mirate più efficaci, come ad esempio gli inibitori di BTK o di BCL-2 in monoterapia o in combinazione con un anticorpo anti-CD205. Si sono quindi affermati due principali paradigmi di trattamento:5
- Trattamento continuativo
- Regimi di combinazione a durata fissa
Le principali classi di farmaci sono:3
- Inibitori di BCL-2 (BCL2i). Questi farmaci sono utilizzati in prima linea, in combinazione con un anti-CD20 o BTKi, in pazienti unfit o anziani sulla base di studi di fase III. I BCL2i sono anche una delle migliori alternative nei pazienti con malattia recidivata/refrattaria e con alto rischio di aberrazioni genomiche.1
- Inibitori della tirosin-chinasi di Bruton (BTKi). Questi farmaci sono spesso raccomandati in prima linea nei pazienti con malattia sintomatica che necessitano di terapia, sulla base di studi di confronto con la terapia standard.1
- Inibitori della fosfatidil-inositolo-3-chinasi (PI3Ki). Rappresentano un’alternativa terapeutica ai BTKi nel trattamento della LLC recidivata/refrattaria, in combinazione con gli anti-CD20. Possono avere un ruolo nei pazienti con cariotipi complessi, con alto rischio di progressione e/o trasformazione se in trattamento con altre terapie o in pazienti anziani che non tollerano bene i BTKi inibitori.1
BCR: recettore delle cellule B; BTKi: inibitori della tirosin-chinasi di Bruton; LLC: leucemia linfatica cronica; PI3Ki: inibitori della fosfatidil-inositolo 3-chinasi; TP53: proteina tumorale 53.
Epidemiologia
La LLC è la leucemia più frequente nel mondo occidentale con un’incidenza di 4,2 casi 100.000 persone/anno.2
- L’età media alla diagnosi è di 72 anni. Circa il 10% dei pazienti affetti da LLC è più giovane di 55 anni.2
- Si osserva un aumento dell’incidenza sopra gli 80 anni pari a 30 casi/100.000/anno.2
- C’è una netta differenza nell’incidenza tra uomini e donne. Negli uomini si riscontrano 6,8 casi/100.000/anno, mentre nelle donne 3,5 casi/100.000/anno.1
- Per quanto riguarda l’origine etnica si riscontrano le seguenti incidenze:1
- Caucasici: 7,3 e 3,8 casi per 100.000/anno per uomini e donne rispettivamente
- Afroamericani: 4,9 e 2,4 casi per 100.000/anno per uomini e donne rispettivamente
- Asiatici: 1,5 e 0,7 casi per 100.000/anno per uomini e donne rispettivamente.
Patogenesi
La causa principale di LLC è la perdita o l’aggiunta di esteso materiale cromosomico seguito da mutazioni addizionali che insorgono successivamente e possono rendere più aggressiva la malattia.3
Tra le modificazioni cromosomiche ad oggi individuate vi sono:3
- Delezione del braccio lungo del cromosoma 13 (del[13q14]). È quella più comunemente riscontrata (55% dei casi) e coinvolge la banda 13q14.3
- Delezione del braccio lungo del cromosoma 11 (del[11q]). Si osserva nel 25% dei casi nei pazienti naïve alla chemioterapia con malattia in stadio avanzato e nel 10% dei pazienti con malattia allo stadio precoce.3
- Trisomia 12. Si osserva nel 10-20% dei pazienti, ma non sono noti i geni coinvolti nella patogenesi della malattia. Il valore prognostico della trisomia 12 è ancora oggetto di dibattito.3
- Delezione del braccio corto del cromosoma 17 (del[17p]). Si osserva nel 5-8% dei pazienti naïve alla chemioterapia.3
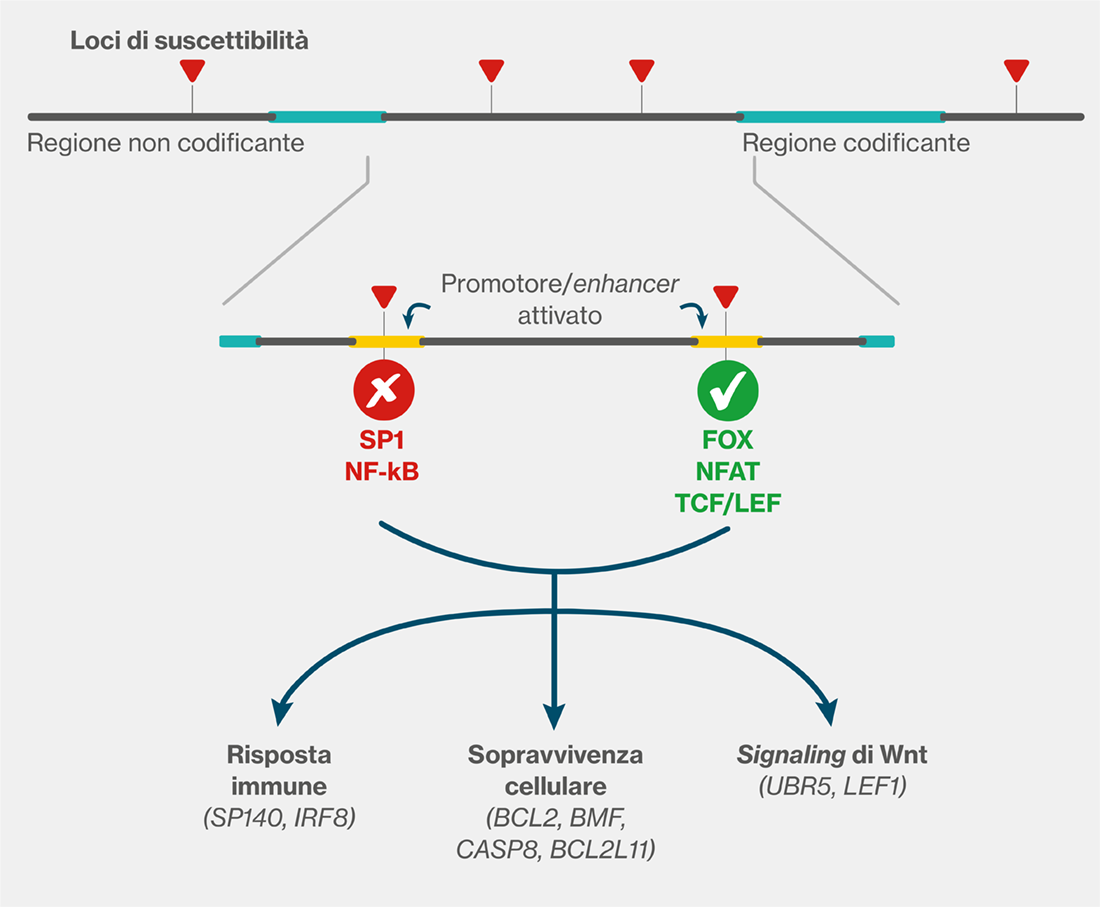
Sono stati identificati 45 loci di suscettibilità soprattutto all’interno di regioni non codificanti del genoma.1 La maggioranza dei loci di suscettibilità (93%) è collocato all’interno di promotori attivi o in regione enhancers e sono responsabili di modificazioni nei siti di legame di numerosi fattori di trascrizione (come FOX, NFAT e TCF/LEF) (Figura 1). Ne risulta un’alterata espressione di più di 30 geni coinvolti nella risposta immunitaria, nella sopravvivenza cellulare o nella via del segnale di Wnt (Figura 2).1,3
Figura 1. Meccanismi genetici di suscettibilità. Tratto da Fig. 1, ref. 1.
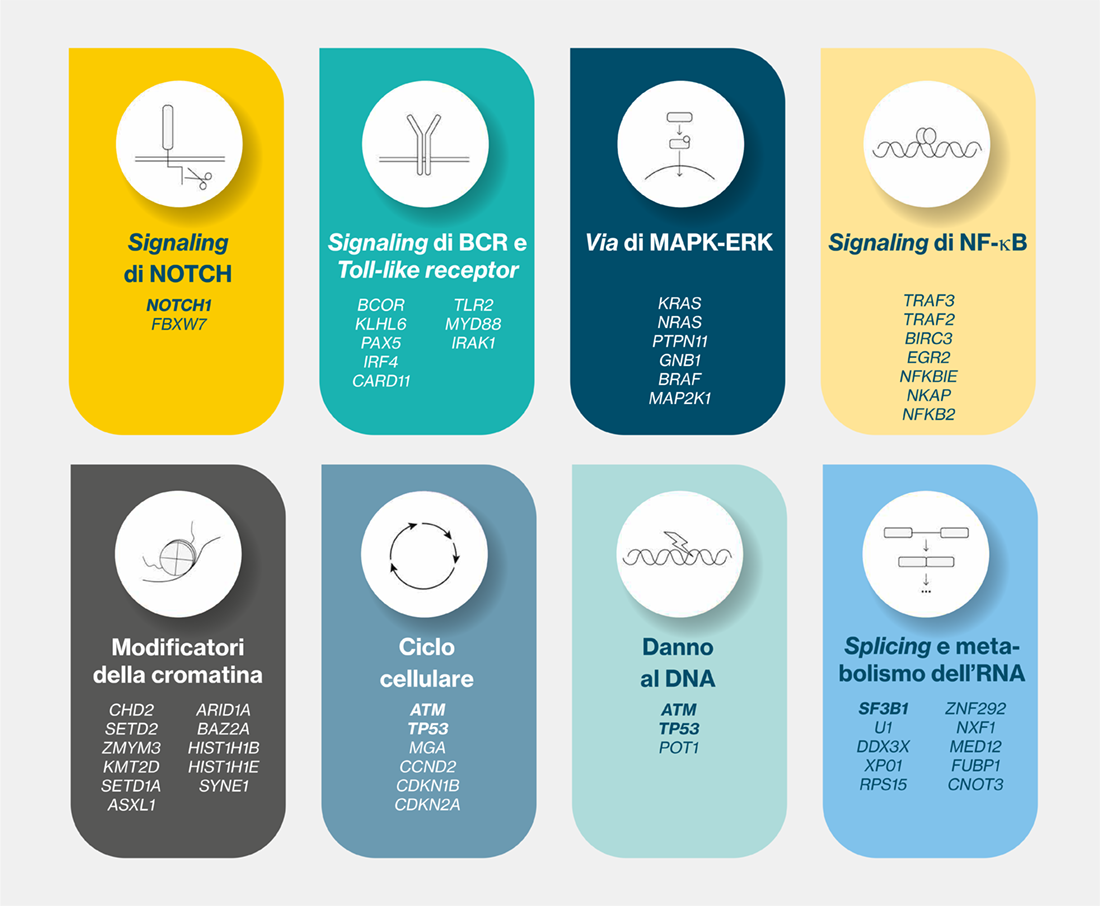
Figura 2. Geni mutati ricorrenti nella LLC e i principali pathway in cui sono coinvolti.
In grassetto sono indicati di geni mutati riscontrati più frequentemente (>5%) nei pazienti di nuova diagnosi. Tratto da Fig. 3, ref. 1.
Il ruolo del microambiente
La sopravvivenza delle cellule LLC dipende soprattutto dalla presenza di un microambiente permissivo che coinvolge la componente cellulare: macrofagi, cellule T e cellule dendritiche stromali follicolari. Queste cellule forniscono stimoli in grado di attivare le vie del segnale di proliferazione e sopravvivenza nelle cellule trasformate. Chemochine, citochine e fattori angiogenici interagiscono con le cellule leucemiche attraverso i recettori di superficie o le molecole di adesione supportando la loro sopravvivenza.3
Fattori di rischio
Al momento non sono noti fattori di rischio modificabili. È stata invece riconosciuta una predisposizione genetica legata all’insorgenza della LLC.2 Avere un parente di primo grado affetto dalla malattia determina un aumento del rischio da 6 a 9 volte.2
La diagnosi della LLC
Criteri diagnostici
Nella maggioranza dei casi la LLC viene diagnosticata mediante conta delle cellule ematiche, conta differenziale, analisi dello striscio di sangue periferico e immuno-fenotipizzazione.1
La diagnosi di LLC è definita in base ai seguenti criteri:3
Si possono osservare anche grandi linfociti atipici o pro-linfociti, ma non devono eccedere del 55%.3 Una percentuale maggiore di pro-linfociti farebbe propendere per una diagnosi di leucemia prolinfocitica (PLL a cellule B).1 Un’ulteriore caratteristica di queste cellule è la presenza di ombreggiature a livello nucleare, dette ombre di Gumprecht che indicano residui di degradazione cellulare.1
Stadiazione
Oggi sono in uso due metodi di stadiazione ampiamente accettati: la stadiazione di Rai e la stadiazione di Binet. Entrambi i metodi identificano tre maggiori gruppi prognostici con outcome clinici discreti. Sono due sistemi semplici, economici, basati sull’esame obiettivo e sui test di laboratorio. Non necessitano di valutazione ecografica, tomografia computerizzata e risonanza magnetica.3
Stadiazione di Rai
La stadiazione di Rai è stata modificata per ridurre il numero dei gruppi prognostici da 5 a 3 e definisce questi livelli di rischio:3
Stadiazione di Binet
La stadiazione di Binet definisce:3
Valutazione del rischio
Al fine di ridurre l’eccesso e la ridondanza delle informazioni prognostiche sono stati elaborati degli score che misurano pochi parametri prognostici essenziali e clinicamente rilevanti. Tali score combinano informazioni di natura clinica, biologica e genetica.3
Al momento, lo score maggiormente rilevante dal punto di vista prognostico è il CLL International Prognostic Index (CLL-IPI) che include cinque fattori prognostici:3
- Delezione e/o mutazione del gene TP53 (anche detta disfunzione TP53),
- Status mutazionale IGHV, β2-microglobulina sierica,
- Stadio clinico
- Età
Il CLL-IPI individua quattro gruppi con diversa sopravvivenza globale a 5 anni (Tabella 1) e permette di identificare in modo più accurato rispetto alla stadiazione clinica i pazienti con LLC che non necessitano di trattamento come i pazienti a basso rischio con CLL-IPI di 0 o 1 e i pazienti con malattia asintomatica.3
Diversi studi hanno dimostrato che in questi pazienti a stadio precoce di malattia il trattamento non apporta ad un beneficio in termini di sopravvivenza. I pazienti asintomatici con una malattia a stadio precoce (Rai 0, Binet A) devono essere monitorati senza trattamento, fino a evidenza di rapida progressione della malattia (Tabella 1).3
La decisione di intraprendere un trattamento dipende dalla presenza di malattia attiva o sintomatica.3
| Categoria CLL-IPI | OS a 5 anni | Potenziali conseguenze cliniche |
| Rischio basso | 93,2% | Non trattare |
| Rischio intermedio | 79,3% | Non trattare a meno che la malattia sia evidentemente sintomatica |
| Rischio elevato | 63,3% | Trattamento indicato a meno che non ci sia malattia asintomatica |
| Rischio molto elevato | 23,3% | Se il trattamento è necessario non utilizzare la chemioterapia ma nuovi agenti o trattamenti utilizzati nei trial clinici |
Tabella 1. Categorie di pazienti in base allo score CLL-IPI. Tratto da Tab. 1, ref. 3.
Classificazione dei pazienti Fit/Unfit
Prima di iniziare il trattamento è importante prendere in considerazione la presenza di comorbilità preesistenti come cardiomiopatie, aritmie, insufficienza renale, l’utilizzo di farmaci concomitanti ed anche le preferenze del paziente relativamente al tipo di trattamento.3
Prima di raccomandare il trattamento devono essere presi in considerazione questi parametri:3
- Stadio clinico della malattia
- Sintomi
- Fitness e malattie concomitanti, con particolare attenzione alla tossicità d’organo
- Rischio genetico di leucemia
- Terapia in atto (prima o seconda linea, risposta vs. non risposta all’ultimo trattamento)
Si definiscono pazienti “Fit” i pazienti con malattia avanzata (Binet C, Rai III-IV) o attiva e sintomatica in buone condizioni fisiche con una clearance della creatinina nella norma CrCl e un basso punteggio alla “cumulative illness rating scale” (CIRS) (Tabella 2).3
PAZIENTI FIT
CIRS ≤6
CrCl ≥70 mL/min
PAZIENTI UNFIT
CIRS >6
CrCl <70 mL/min
e/o
presenza di comorbilità
Tabella 2. Classificazione dei pazienti in base allo stato di salute. Elaborazione grafica da testo, ref. 3.
CLL-IPI: CLL International Prognostic Index; del: delezione; Hb: emoglobina; IGHV: gene della regione variabile della catena pesante delle immunoglobuline; LLC: leucemia linfatica cronica; PLL: leucemia prolinfocitica; TP53: proteina tumorale 53
In evidenza
Risorse aggiuntive
Bibliografia
- Delgado J, et al. Haemaologica. 2020;105(9):220-2217
- Eichhorst B, et al, Ann. Oncol. 2021; 32(1):23-33
- Hallek M. AM J Hematol 2019;94(11):1266-1287
- ESMO 2024
- Awan FT, et al. AM soc Clin Oncol Educ Book 2020
Codice aziendale: IT-ONCC-250001
Data di ultimo aggiornamento: Settembre 2025