VENCLYXTO har en hanterbar säkerhetsprofil vid AML1,2
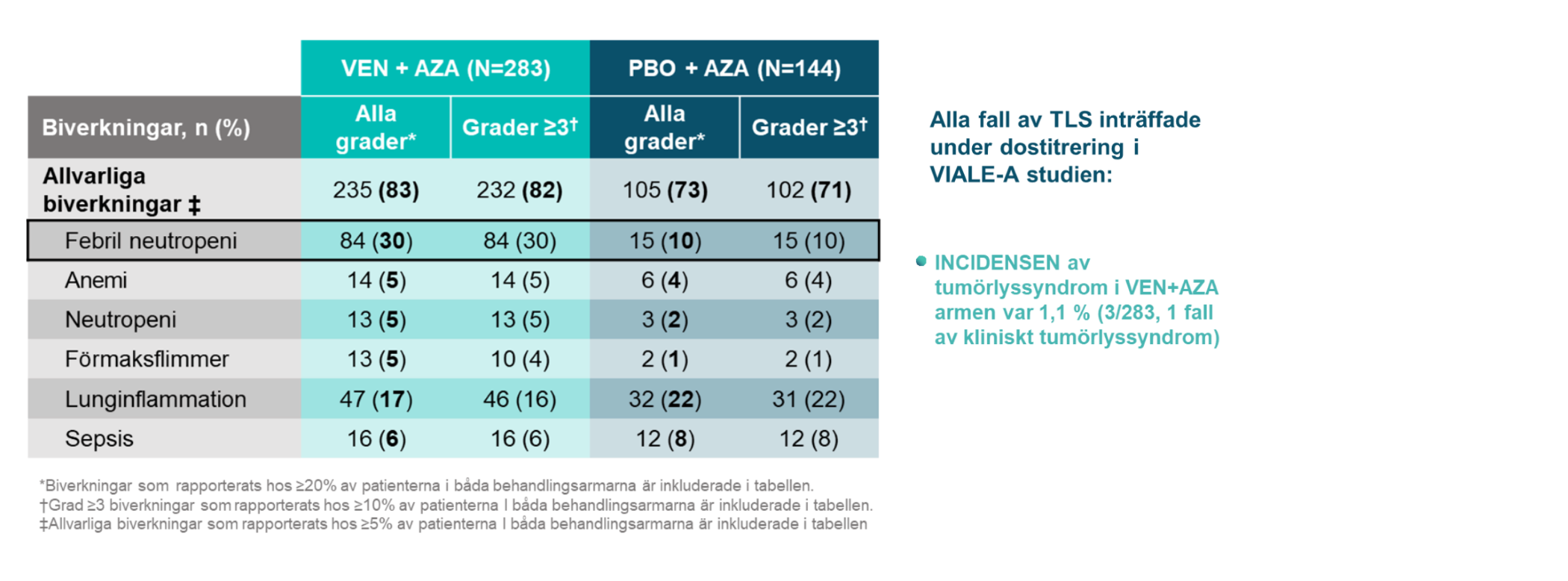
VENCLYXTO kan orsaka en snabb minskning av tumörbördan, vilket medför en risk för tumörlyssyndrom vid insättning och under dostitreringsfasen.
Alla patienter ska utvärderas med avseende på risk och ska ges lämplig profylaktisk behandling mot TLS inklusive hydrering och läkemedel mot hyperurikemi.
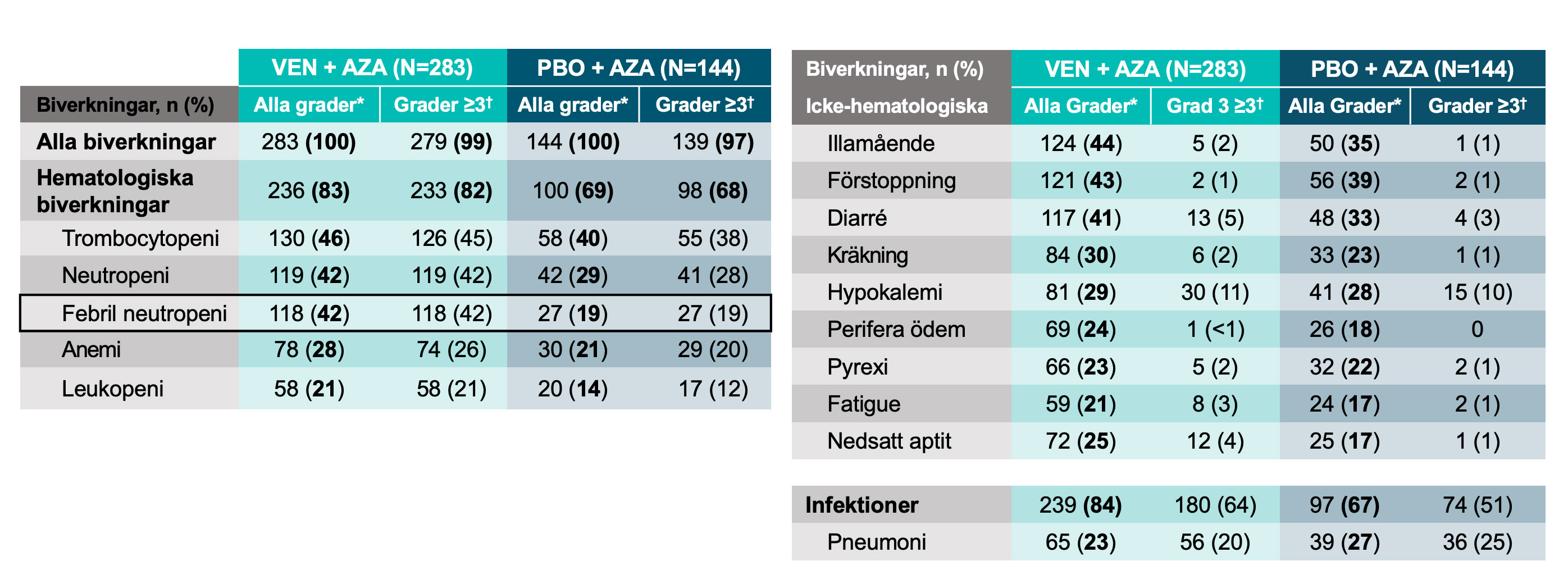
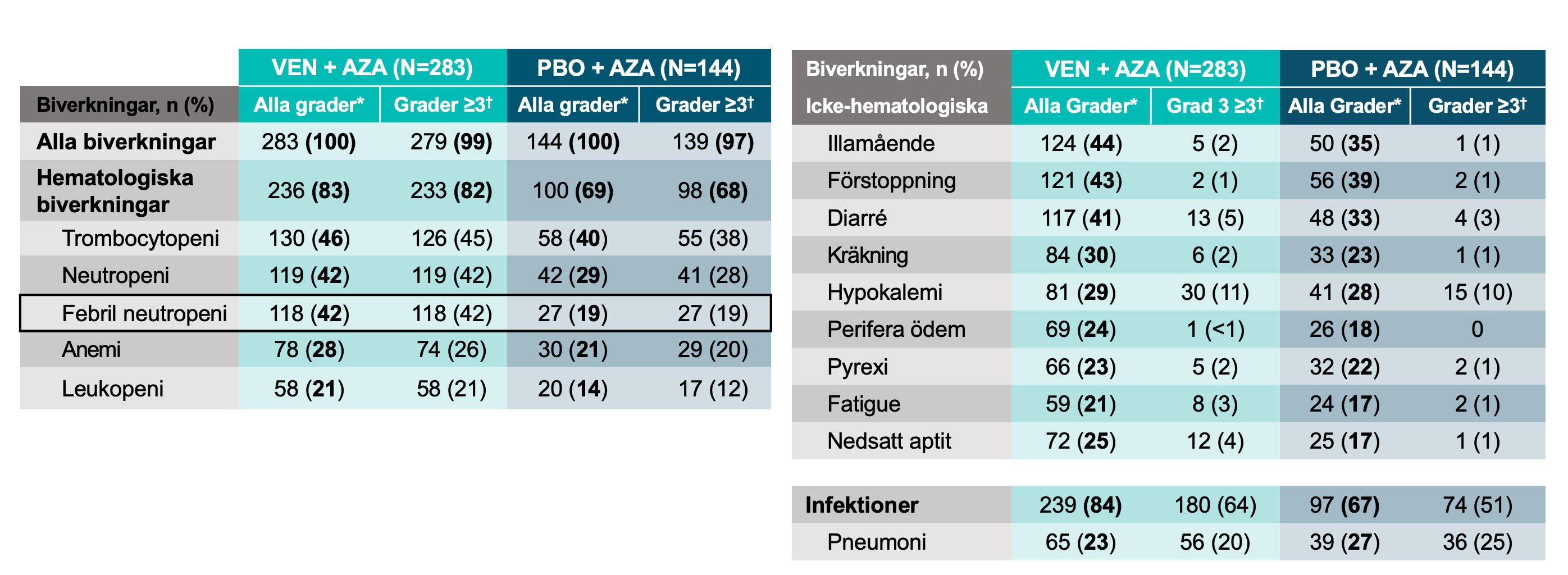
I VIALE‑A-studien var de vanligast förekommande biverkningarna (≥ 20 %) oavsett grad hos patienterna som fick VENCLYXTO i kombination med azacitidin trombocytopeni, neutropeni, febril neutropeni, illamående, diarré, kräkning, anemi, trötthet, lunginflammation, hypokalemi och nedsatt aptit.
De vanligast rapporterade allvarliga biverkningarna (≥ 5 %) hos patienterna som fick VENCLYXTO i kombination med azacitidin var febril neutropeni, lunginflammation, sepsis och blödning.
Ytterligare säkerhetsaspekter samt läkemedelsinteraktioner vid AML1
- Överkänslighet mot den aktiva substansen eller mot något hjälpämne
- Samtidig användning av preparat med Johannesört
- Patienter med nedsatt njurfunktion (CrCl <80 ml/min) kan behöva intensivare förebyggande behandling och övervakning för att minska risken för TLS (tumörlyssyndrom) vid behandlingsstart och under dostitreringsfasen). VENCLYXTO ska endast ges till patienter med kraftig njurfunktionsnedsättning (CrCl ≥ 15 ml/min och < 30 ml/min) om fördelen med behandlingen överväger riskerna. Patienterna ska övervakas noggrant för tecken på toxicitet på grund av den ökade risken för TLS.
- Ingen dosjustering behövs för patienter med milt, måttligt eller svårt nedsatt njurfunktion (CrCl ≥ 15 ml/min och < 90 ml/min).
- Läs mer på www.fass.se.
- Inga dosjusteringar rekommenderas för patienter med lätt till måttlig leverfunktionsnedsättning. Patienter med måttlig leverfunktionsnedsättning ska övervakas noggrannare avseende tecken på toxicitet vid behandlingsstart och under dostitreringsfasen.
- En dosminskning på minst 50 % under hela behandlingstiden rekommenderas för patienter med gravt nedsatt leverfunktion. Dessa patienter ska övervakas noggrannare för tecken på toxicitet.
- Läs mer på www.fass.se
- För patienter som kräver samtidig användning av VENCLYXTO och starka CYP3A-hämmare (t.ex. itrakonazol, ketokonazol, posakonazol) eller måttliga CYP3A-hämmare (t.ex. ciprofloxacin, erytromycin, flukonazol,) ska VENCLYXTO administreras enligt tabell 7 i www.fass.se.
- Patienterna ska övervakas noggrannare avseende tecken på toxicitet och ytterligare dosjusteringar kan komma att krävas. Den dos av VENCLYXTO som användes innan CYP3A-hämmaren sattes in ska återupptas 2 till 3 dagar efter att hämmaren har satts ut.
- Produkter med grapefrukt, pomerans och stjärnfrukt (carambola) ska undvikas under behandling med VENCLYXTO eftersom de innehåller CYP3A-hämmare.
- Samtidig användning av VENCLYXTO och starka CYP3A-inducerare (t ex karbamazepin, fenytoin) eller måttliga CYP3A-inducerare (t ex bosentan, efavirenz) ska undvikas. Alternativa behandlingar med lägre CYP3A-inducerande aktivitet ska övervägas.
Vill du hålla dig informerad om nyheter och inbjudningar från AbbVie Hematologi?
Vill du veta mer om Venclyxto?
Referens: 1. DiNardo CD, et al. N Engl J Med. 2020;383(7):617-29. 2. VENCLYXTO Produktresumé 24 jul 2025.