Επειδή η φάση «ON» είναι η δική τους ώρα
Λίστα ελέγχου ασθενών
Το Duodopa® ενδείκνυται ως θεραπευτική αγωγή για την προχωρημένη νόσο Πάρκινσον που αποκρίνεται στη levodopa με σοβαρής μορφής κινητικές διακυμάνσεις και υπερκινησία ή δυσκινησία όταν οι διαθέσιμοι συνδυασμοί φαρμακευτικών προϊόντων για τη νόσο Πάρκινσον δεν έχουν δώσει ικανοποιητικά αποτελέσματα.1
Κλινικά χαρακτηριστικά προχωρημένης νόσου Πάρκινσον
Μια επιτροπή 17 ειδικών στις κινητικές διαταραχές από 10 χώρες κατάφερε να διατυπώσει μια συναινετική δήλωση, ορίζοντας 15 κλινικά χαρακτηριστικά που βοηθούν στην αναγνώριση της προχωρημένης νόσου Πάρκινσον.12
Διαγνωστικό εργαλείο
Από τα 15 χαρακτηριστικά, 3 έχουν προταθεί ως διαγνωστικό εργαλείο, τα κριτήρια 5-2-1:
- Λήψη τουλάχιστον 5 από στόματος δόσεων levodopa ημερησίως
- Τουλάχιστον 2 ώρες σε φάση «OFF» ημερησίως
- Τουλάχιστον 1 ώρα ενοχλητικής υπερκινησία ημερησίως
Η παρουσία τουλάχιστον ενός από τα παραπάνω κριτήρια 5-2-1 μπορεί να αποτελεί ένδειξη προχωρημένης νόσου Πάρκινσον.
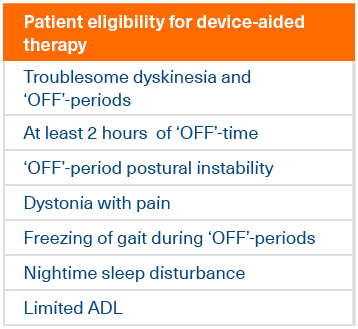
Κλινικά χαρακτηριστικά για τεχνολογικά υποβοηθούμενη θεραπεία
Η ίδια επιτροπή ειδικών στις κινητικές διαταραχές βελτίωσε περαιτέρω το διαγνωστικό εργαλείο, καταλήγοντας σε 7 κλινικά χαρακτηριστικά των ατόμων με προχωρημένη νόσο Πάρκινσον που τους κάνει κατάλληλους για τεχνολογικά υποβοηθούμενη θεραπεία, όπως το Duodopa®.12
Αυτά τα κλινικά χαρακτηριστικά μπορεί να λειτουργήσουν ως ένας χρήσιμος οδηγός ελέγχου όταν αξιολογείτε τους ασθενείς που μπορεί να είναι κατάλληλοι για θεραπεία με Duodopa®.
Η παρουσία οποιουδήποτε κλινικού χαρακτηριστικού (εκτός του περιορισμού των δραστηριοτήτωντης καθημερινής ζωής, που προϋποθέτει την παρουσία επιπλέον κλινικού χαρακτηριστικού) μπορεί να αποτελεί ένδειξη καταλληλότητας για τεχνολογικά υποβοηθούμενη θεραπεία.
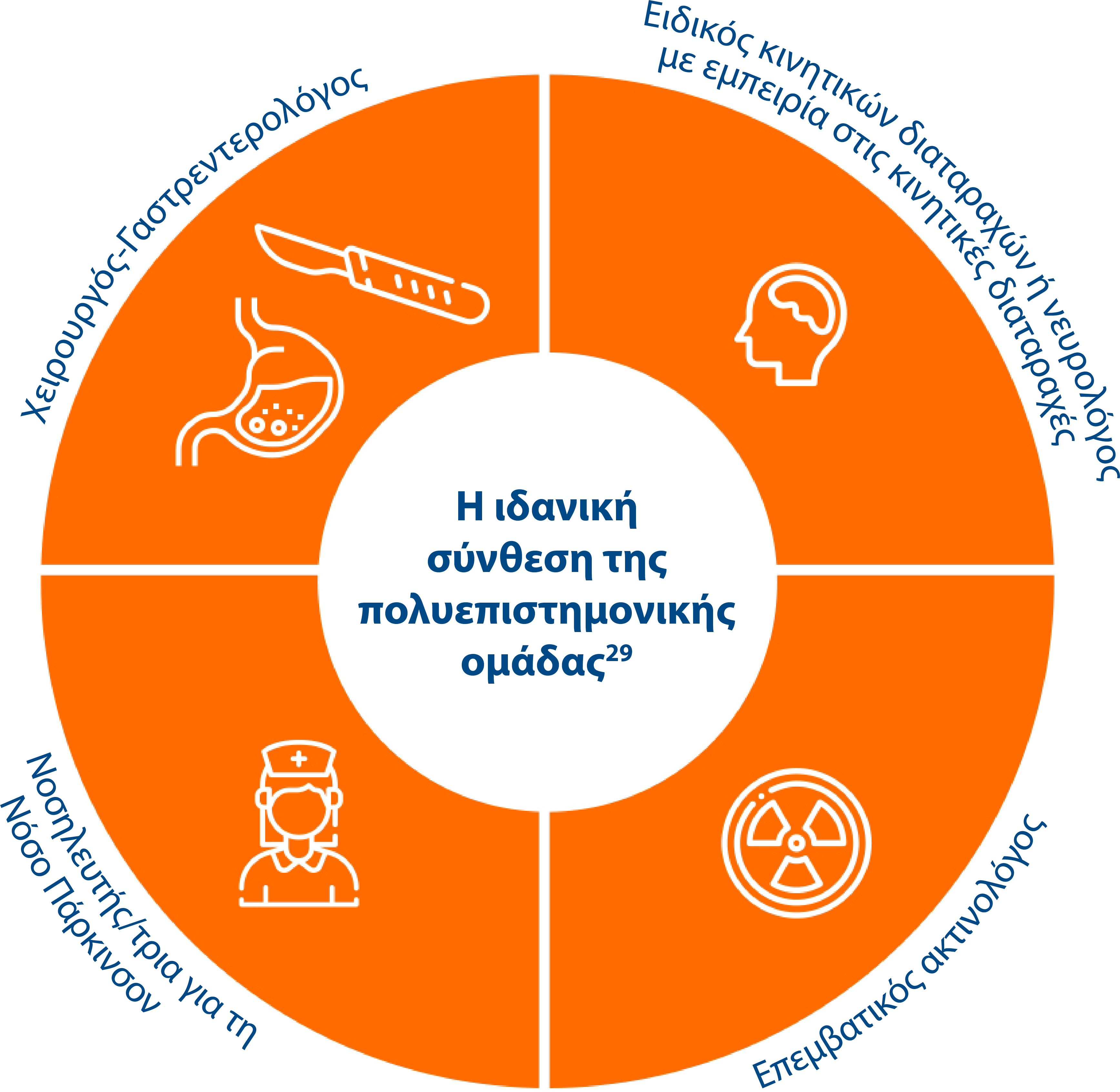
Η συνεργασία και η ομαδική προσπάθεια έχουν μεγάλη σημασία
H συγκρότηση μιας συνεργατικής και σαφώς δομημένης πολυεπιστημονικής ομάδας βοηθάει στην αντιμετώπιση των δυκολιών του νοσήματος.29
Ανάλογα με την πρακτική που εφαρμόζεται κατά τόπους είναι επίσης δυνατή η συμμετοχή και άλλων επαγγελματιών υγείας στην πολυεπιστημονική ομάδα. 30
Η καλή επικοινωνία μεταξύ ιατρού και ασθενή μπορεί να πετύχει, πλέον των άμεσα θεραπευτικών αποτελεσμάτων, συμμόρφωση στη θεραπεία, αμοιβαία κατανόηση και εμπιστοσύνη, τα οποία σχετίζονται με την βελτίωση στην εν γένει υγεία του ασθενή. 31
Έλεγχος ανταπόκρισης στη θεραπεία με Duodopa® πριν τη χειρουργική επέμβαση
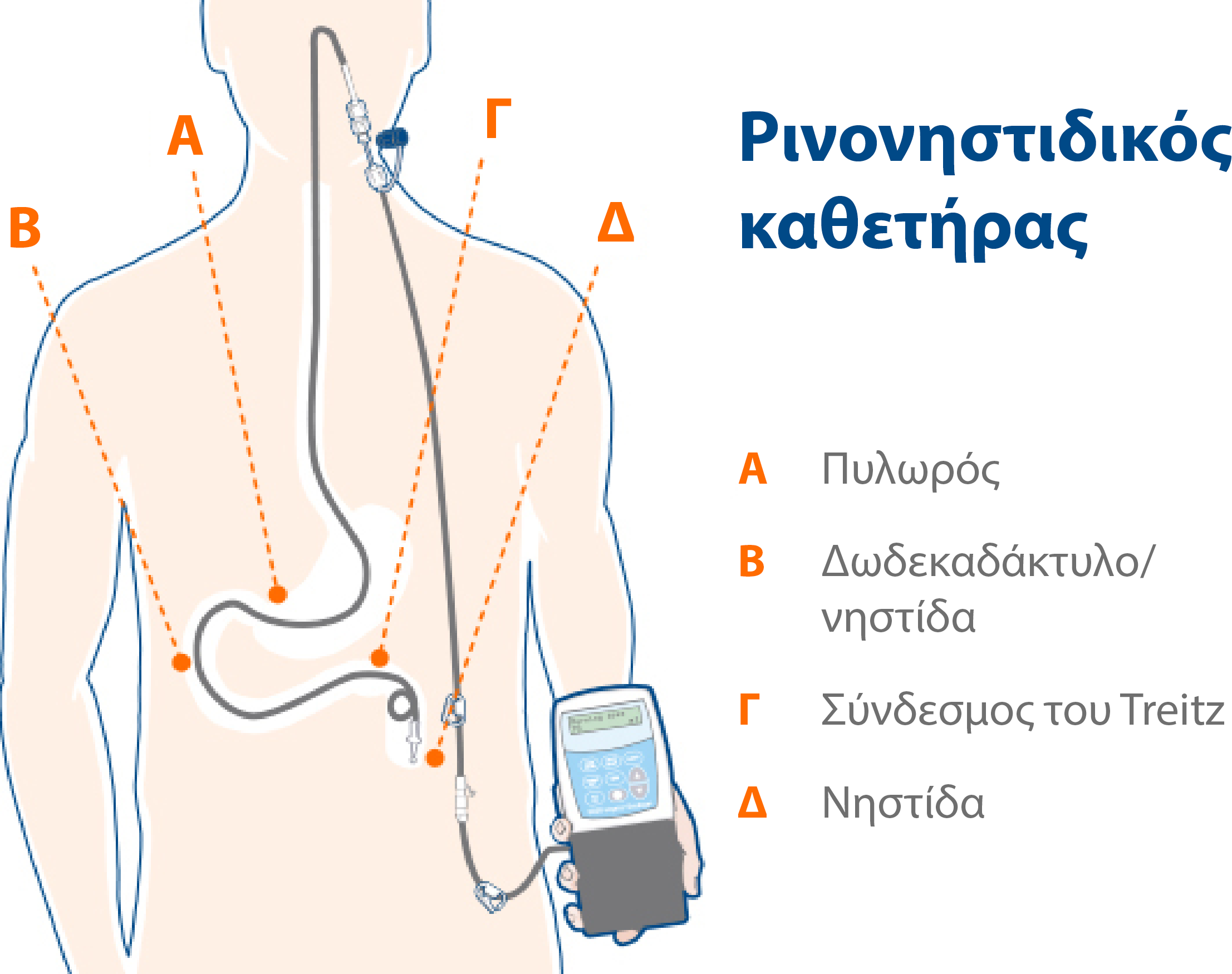
Πριν τη δημιουργία μόνιμης διαδερμικής ενδοσκοπικής γαστροστομίας και την τοποθέτηση νηστιδικού καθετήρα (PEG-J) θα πρέπει να ληφθεί υπόψη η χρήση προσωρινού ρινοδωδεκαδακτυλικού/ρινονηστιδικού καθετήρα για να εξακριβωθεί εάν ο ασθενής ανταποκρίνεται θετικά σε αυτή την μέθοδο θεραπείας.1
Μέσω του ρινονηστιδικού καθετήρα, το Duodopa® χορηγείται απευθείας στη νηστίδα. Αυτή η δοκιμαστική φάση μπορεί να διαρκέσει περίπου 5 ημέρες.30
Σε μια προοπτική μελέτη, 91,5% των ασθενών οι οποίοι ολοκλήρωσαν τη δοκιμαστική φάση εισαγωγής ρινονηστιδικού καθετήρα προχώρησαν σε τοποθέτηση σωλήνα γαστρονηστιδοστομίας7 .
Σε περιπτώσεις, στις οποίες ο ιατρός θεωρεί ότι αυτή η αξιολόγηση δεν είναι απαραίτητη, η δοκιμαστική φάση εισαγωγής ρινονηστιδικού καθετήρα μπορεί να παρακαμφθεί και η θεραπεία να ξεκινήσει απευθείας με τοποθέτηση του καθετήρα γαστρονηστιδοστομίας1.
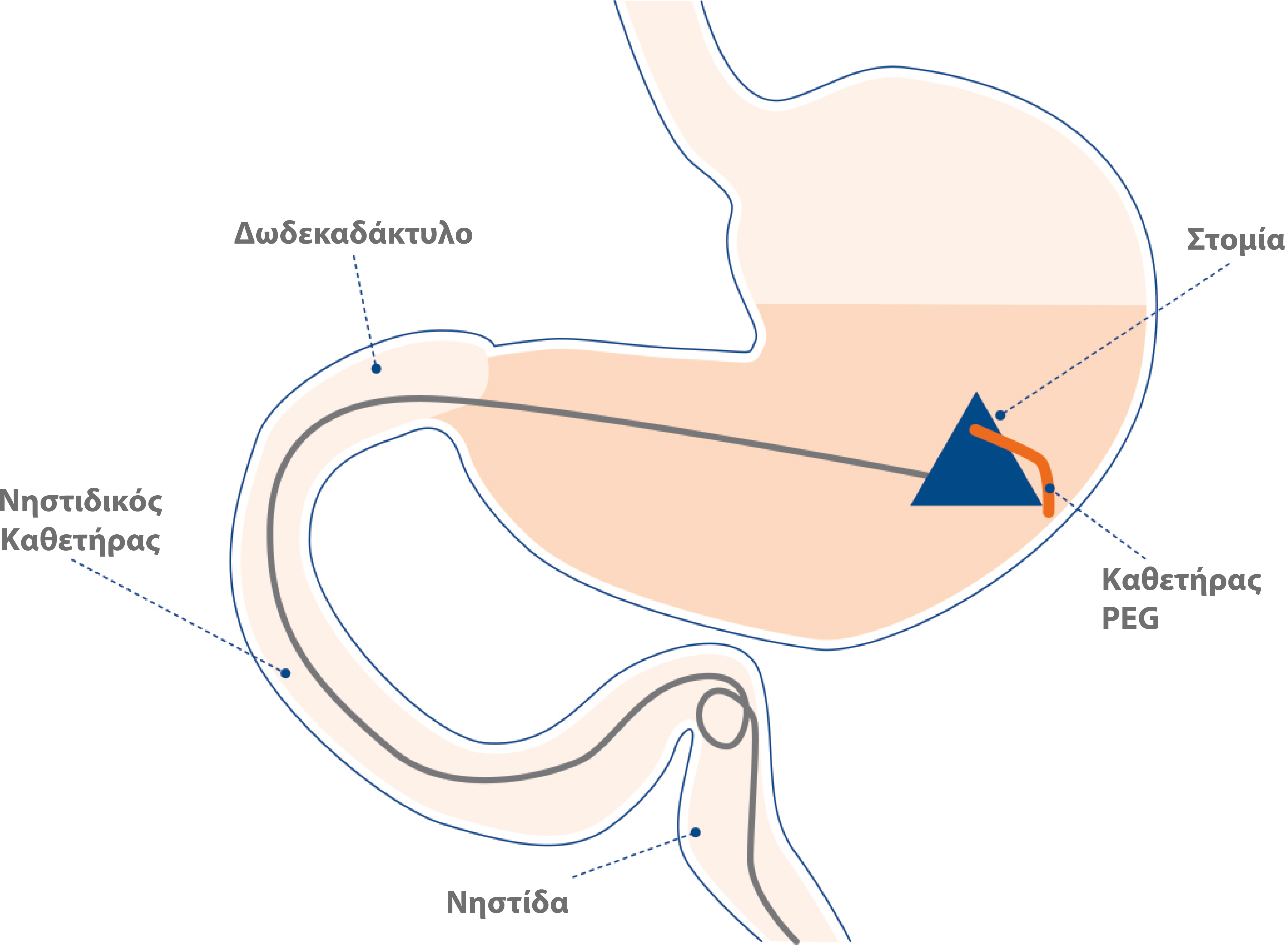
Συνοπτική παρουσίαση της διαδικασίας εισαγωγής γαστρονηστιδοστομίας
Η έναρξη της θεραπείας Duodopa® με τη διαδικασία PEG-J χωρίζεται σε πέντε σημαντικά βήματα:
1. Προετοιμασία
των ασθενών, η οποία περιλαμβάνει στοματική υγιεινή, αντιβιοτική προφύλαξη σύμφωνα με το πρωτόκολλο του κέντρου, και τοποθέτησή τους σε ύπτια θέση23
2. Tοποθέτηση του καθετήρα γαστρονηστιδοστομίας
με προσδιορισμό της κατάλληλης θέσης παρακέντησης, παρακέντηση του στομάχου και εισαγωγή της κάνουλας παρακέντησης υπό ενδοσκοπικό έλεγχο. Eισαγωγή του νήματος-οδηγού, στερέωση του καθετήρα PEG στο νήμα-οδηγό και έλξη και των δύο διαμέσω του κοιλιακού τοιχώματος έως ότου το εσωτερικό καθηλωτικό στερέωσης βρεθεί σε άμεση επαφή με το εσωτερικό γαστρικό τοίχωμα, και ασφάλιση του καθετήρα γαστρονηστιδοστομίας PEG23
3. Στερέωση του συνδετικού σχήματος -Υ
στον καθετήρα γαστρονηστιδοστομίας PEG24
4. Τοποθέτηση του νηστιδικού καθετήρα "J"
και εισαγωγή αυτού στο συνδετικό σχήμα -Υ 24
5. Στερέωση & προσαρμογή του νηστιδικού καθετήρα "J" στο καθετήρα γαστρονηστιδοστομίας PEG
–Η αντλία είναι πλήρως συνδεδεμένη και μπορεί να ξεκινήσει η θεραπεία Duodopa®23
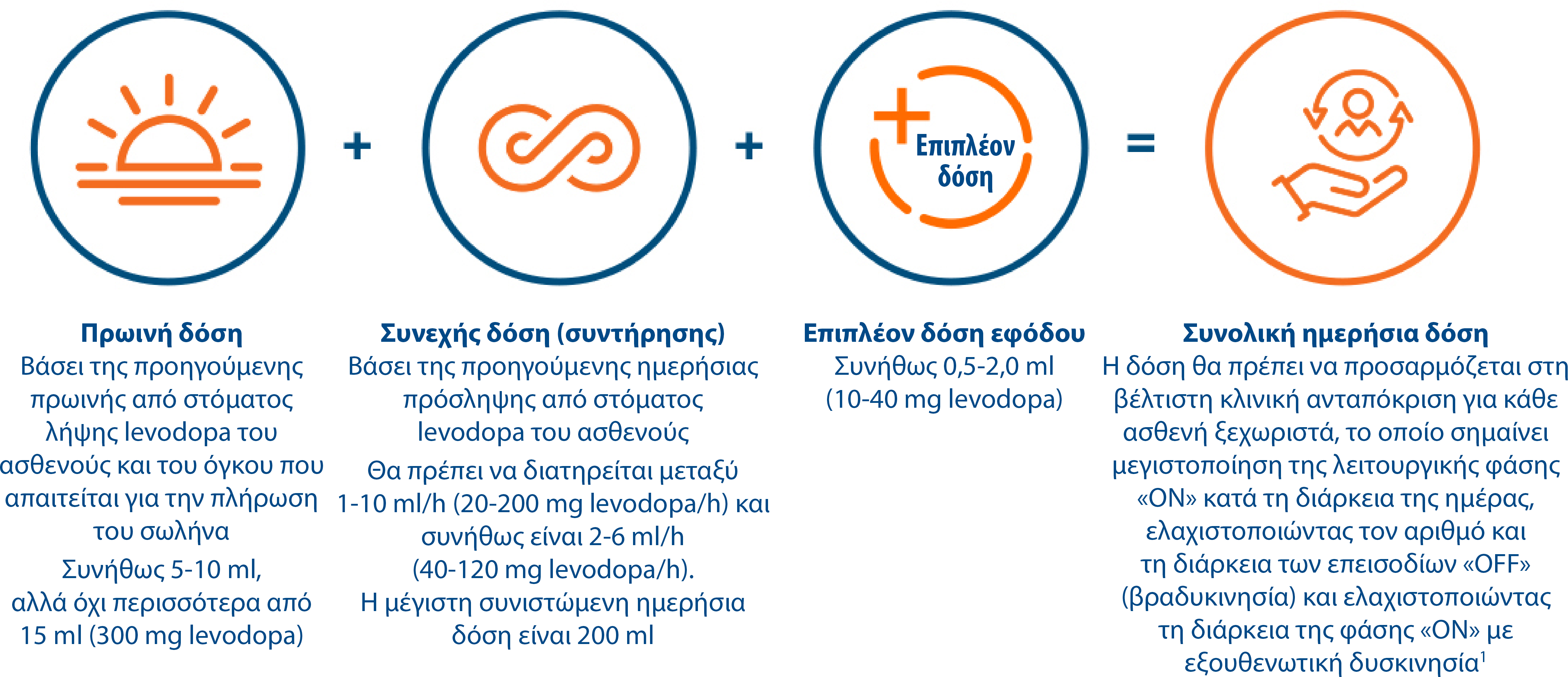
Υπολογισμός και τιτλοποίηση της δόσης του Duodopa®
Η δόση του Duodopa® αποτελείται από τρεις εξατομικευμένα προσαρμοσμένες δόσεις, οι οποίες παρέχουν συνεχή θεραπεία για έως και 16 ώρες. 1*
Μετά την έναρξη της θεραπείας, θα πρέπει να πραγματοποιούνται λεπτές προσαρμογές σε αυτές τις τρεις επιμέρους δόσεις της συνολικής δοσολογίας σε διάστημα μερικών εβδομάδων, προκειμένου να επιτυγχάνεται η ιδανική δόση. 1
* Η θεραπεία συνήθως χορηγείται κατά τη διάρκεια των ωρών που οι ασθενείς είναι ξύπνιοι. Εάν δικαιολογείται ιατρικά, το Duodopa® μπορεί να χορηγηθεί έως και για 24 ώρες1
- Περίληψη των Χαρακτηριστικών του Προϊόντος για το Duodopa (εντερική γέλη λεβοντόπα/καρβιντόπα).
- Olanow CW et al. Lancet Neurol 2014;13(2):141 -149.
- Fernandez HH et al. Mov Disord 2018; 33(6):928-936.
- Lopiano L et al. J Neurol 2019; 266:2164-2176.
- Nyholm D et al. Neurology 2005; 64(2):216-223.
- Kruger R et al. Adv Ther 2017; 34(7):1741-1752.
- Fernandez HH et al. Mv Disord 2015;30(4):500-9.
- Antonini A et al. Neurodegen Dis Manag 2018;8(3):161-170.
- Slevin JT et al. J Parkinson’s Dis 2015; 5(1):165-174.
- https://www.ema europa.eu/en/ medicmes/human/orphan-designations/ eu30i035. Accessed 24 November 2020.
- LCIG Worldwide Marketing Authorization Status. Revised 20 October 2020. Data on file.
- Antonini A et a I. Curr Med Res Opin 2018; 34(12):2063-2073.
- Santos-Garcia D et al. Parkinsons Dis 2020:2020:7537924.
- Nyholm D. Parkinsonism Relat Disord 2007; 13(suppl):S13-S17.
- Nyholm D et al. AAPSJ 2013; 15(2):316-323.
- Hughes AJ et al. J Neurol Neurosurg Psychiatry 1992; 55:181-184.
- Goetz CG etal. Mov Disord 2004; 19(9):1020-1028.
- Fox SH et al. Mov Disord 2018; 33(8):1248-1266.
- Varanese S et al. Parkinsons Dis 2011; 2010:480260.
- Kulisevsky J et al. Neurologia 2013; 28(9):558-583.
- Fasano Aet al. BMC Neurology 2019; 19:50.
- Giugni JC, Okun MS. Curr Opin Neurol 2014; 27(4):450-460.
- Οδηγίες χρήσης, AbbVie Εντερικός Καθετήρας 9 FR PEG για 15 και 20 FR, Νοέμβριος 2020
- Οδηγίες χρήσης, AbbVie Κιτ διαδερμικής Ενδοσκοπικής Γαστροστομίας 15 FR / 20 FR, Νοέμβριος 2020
- Οδηγίες χρήσης, AbbVie Ρινονηστιδικός καθετήρας με στυλεό μόνο για εντερική χρήση, Νοέμβριος 2020
- Smiths Medical CADD Legacy® 1400 Operations΄Manual Εγχειρίδιο Λειτουργίας του Legacy Duodopa.
- Φύλλο Οδηγιών Χρήσης του Προϊόντος Duodopa (ΦΟΧ), Ιούνιος 2021
- Antοnini A et al Curr Med ResOpin 2018; 34(12)2063-2073
- Van der Marck MA & Bloem BR. Parkinsonism Relat Disord 2014; Suppl. 1 :S167-S173.
- Pedersen SW et al. Open Neurol 2012; 6:37-50.
- Bell RA et al. J Gen Intern Med 2002; 17(11 ):817-824.
- Markland D et al. J Social Clin Psychol 2005; 26(6):811 -831.
- Street RL et al. Patient Educ Couns 2009; 74(3): 295-301.