Note to affiliates: This update to the venetoclax CLL AbbVie Pro site includes a homepage headline, updated CLL14 6-year, CLL13 4-year, MURANO 7-year data sets, and other streamlined content updates. CLL 13 4-year update reflects the CLL13 data from the Lancet Oncology publication. The CLL14 6-year and MURANO 7-year data have been updated based on the EHA 2023 abstracts. For countries that cannot use these data sets, please follow local regulations and MRLO guidance, and revert to CLL14 5-year and MURANO 5-year published data from the product label.
Primary analysis in ITT population for VEN+O vs O+Clb1:
INV-assessed PFS†: Reduced risk of progression or death (HR=0.35; 95% CI: 0.23–0.53 [P<0.0001]).
| • | Median follow-up of 28 months |
Additional analyses:
6-year PFS estimate (INV-assessed)2‡: 53% vs 22% (HR=0.40; 95% CI: 0.31–0.52) after 5 years off treatment.
| • | Median PFS of 76.2 months with VEN+O vs 36.4 months with O+Clb |
INV-assessed complete remission (CR/CRi)1: 50% vs 23% (P<0.0001).
| • | ORR: 85% (95% CI: 79.2–89.2) vs 71% (95% CI: 64.8–77.2 [P=0.0007]) |
Primary analysis in ITT population for VEN+R vs BR1:
INV-assessed PFS†: Reduced risk of progression or death (HR=0.17; 95% CI: 0.11–0.25 [P<0.0001]).
| • | Median follow-up of 23.8 months |
Additional analyses:
7-year PFS estimate (INV-assessed)3‡: 23% (HR=0.23; 95% CI: 0.18–0.29) vs NE after ~5 years off treatment.
| • | Median PFS of 54.7 months with VEN+R (95% CI: 52.3–59.9) vs 17.0 months with BR (95% CI: 15.5–21.7) |
INV-assessed complete remission (CR/CRi)1‡: 27% vs 8%.
| • | ORR: 93% (95% CI: 88.8–96.4) vs 68% (95% CI: 60.6–74.2) |
*See full dosing information for VEN+O and for VEN+R in the dosing and administration section.
†Primary endpoint.
‡Results are descriptive only.
1L=first line; CLL=chronic lymphocytic leukaemia; VEN+O=VENCLYXTO + obinutuzumab; ITT=intent to treat; O+Clb=obinutuzumab + chlorambucil; INV=investigator; PFS=progression-free survival; HR=hazard ratio; CI=confidence interval; CR=complete remission; CRi=complete remission with incomplete bone marrow recovery; ORR=overall response rate; 2L+=second line + later lines of therapy; VEN+R=VENCLYXTO + rituximab; BR=bendamustine + rituximab; NE=not evaluable.
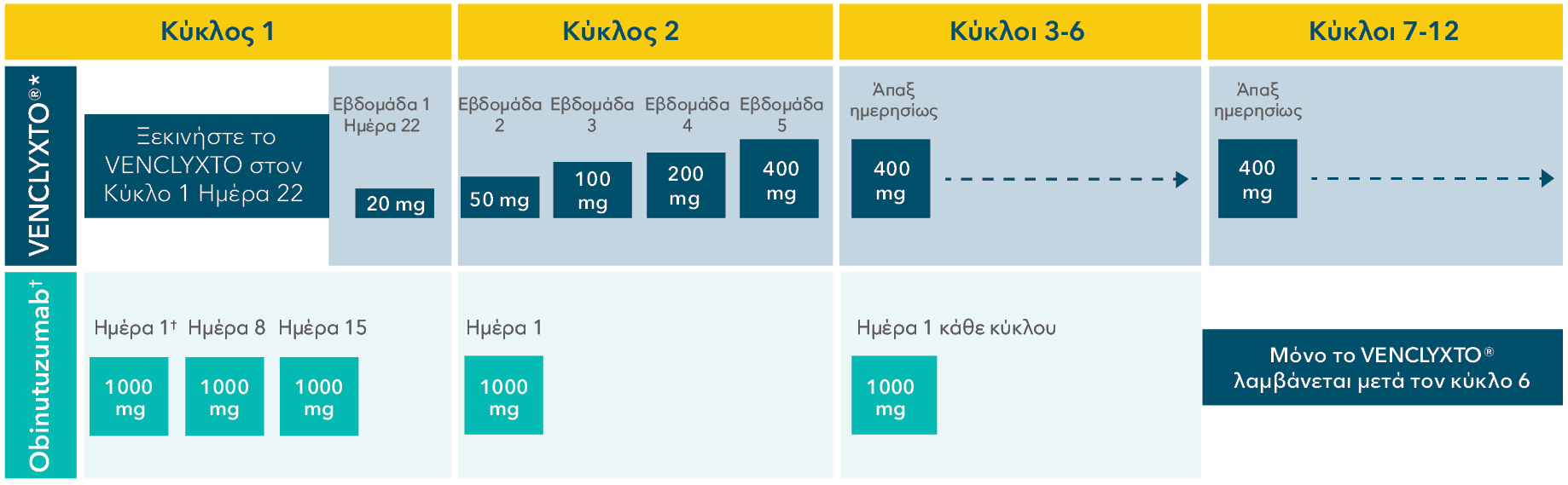
ΣΧΗΜΑΤΑ ΓΙΑ ΣΤΑΘΕΡΟ ΔΙΑΣΤΗΜΑ ΧΟΡΗΓΗΣΗΣ ΣΕ 1L ΧΛΛ1
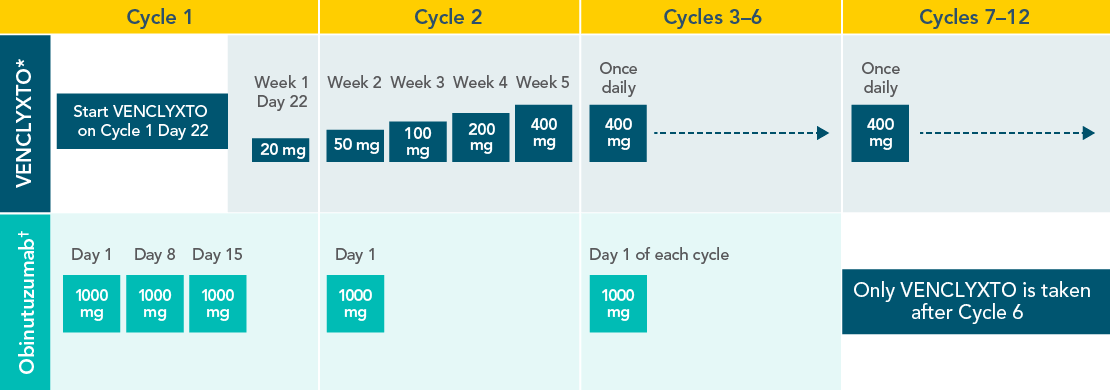
1L CLL: ο συνδυασμός VENCLYXTO® + obinutuzumab έχει σχεδιαστεί να ολοκληρώνεται σε 1 έτος
*Oral tablet.
†Administer intravenously. Dose may be split as 100 mg and 900 mg on Days 1 and 2 of Cycle 1, respectively. Graphic not to scale. Each cycle is 28 days.
*Oral tablet.
†Administer intravenously.
Each cycle is 28 days.
*Από του στόματος θεραπεία.
†Ενδοφλέβια χορήγηση. 100 mg Obinituzumab την Ημέρα 1 του Κύκλου 1,
ακολουθούμενη από 900 mg τα οποία μπορούν να χορηγηθούν την Ημέρα 1 ή την Ημέρα 2.
Κάθε κύκλος είναι 28 ημέρες.
Το σχήμα τιτλοποίησης της δόσης του VENCLYXTO® διάρκειας 5 εβδομάδων, που ξεκινά από τον Κύκλο 1, Ημέρα 22, σχεδιάστηκε ώστε να μειώνει σταδιακά το φορτίο του όγκου (μείωση του όγκου) και ελαττώνει τον κίνδυνο για TLS.
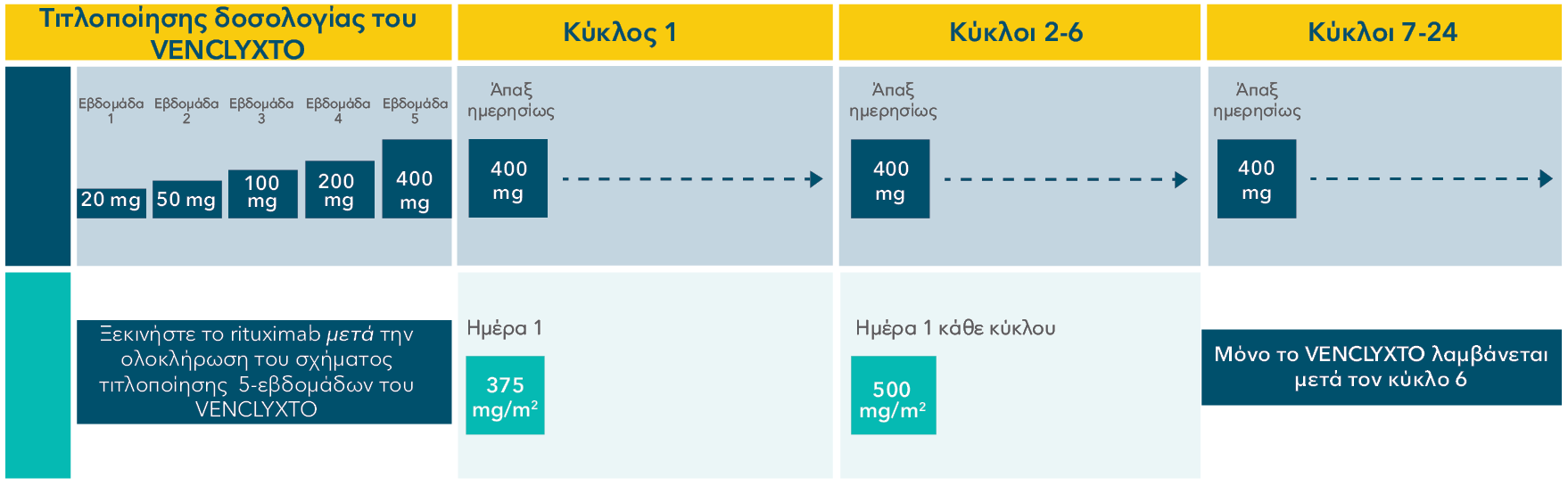
ΣΤΑΘΕΡΟ ΔΙΑΣΤΗΜΑ ΧΟΡΗΓΗΣΗΣ ΣΕ 1L ΚΑΙ 2L + CLL1
2L+CLL: ο συνδυασμός VENCLYXTO® + rituximab έχει σχεδιαστεί να ολοκληρώνεται σε 2 έτη
**Από του στόματος θεραπεία.
+Ενδοφλέβια χορήγηση.
Κάθε κύκλος είναι 28 ημέρες.
Το αρχικό σχήμα τιτλοποίησης της δόσης διάρκειας 5 εβδομάδων σχεδιάστηκε για να μειώσει σταδιακά το φορτίο του όγκου και να ελαττώσει τον κίνδυνο για TLS.
Η ταυτόχρονη χορήγηση του VENCLYXTO® με ισχυρούς ή μέτριους αναστολείς του CYP3A αυξάνει την έκθεση στο VENCLYXTO® και μπορεί να αυξήσει τον κίνδυνο για TLS κατά την έναρξη και κατά τη διάρκεια της φάσης τιτλοποίησης της δόσης. Οι αναστολείς της P-gp ή της BCRP μπορούν επίσης να αυξήσουν την έκθεση στο VENCLYXTO®.
CYP3A=κυττόχρωμα P450 3A, P-gp=P-γλυκοπρωτεϊνη, BCRP=πρωτεϊνη ανθεκτικότητας στον καρκίνο του μαστού.
Με ενδιαφέρει η βελτιωμένη
πρόγνωση ασθενών
Με ενδιαφέρει να προσφέρω
θεραπείες πεπερασμένης διάρκειας
ΠΑΡΑΠΟΜΠΕΣ: 1. VENCLYXTO® Περίληψη Χαρακτηριστικών του Προϊόντος (ΠΧΠ), Αύγουστος 2023.