LEUCEMIA MIELOIDE AGUDA (LMA)
Diagnóstico
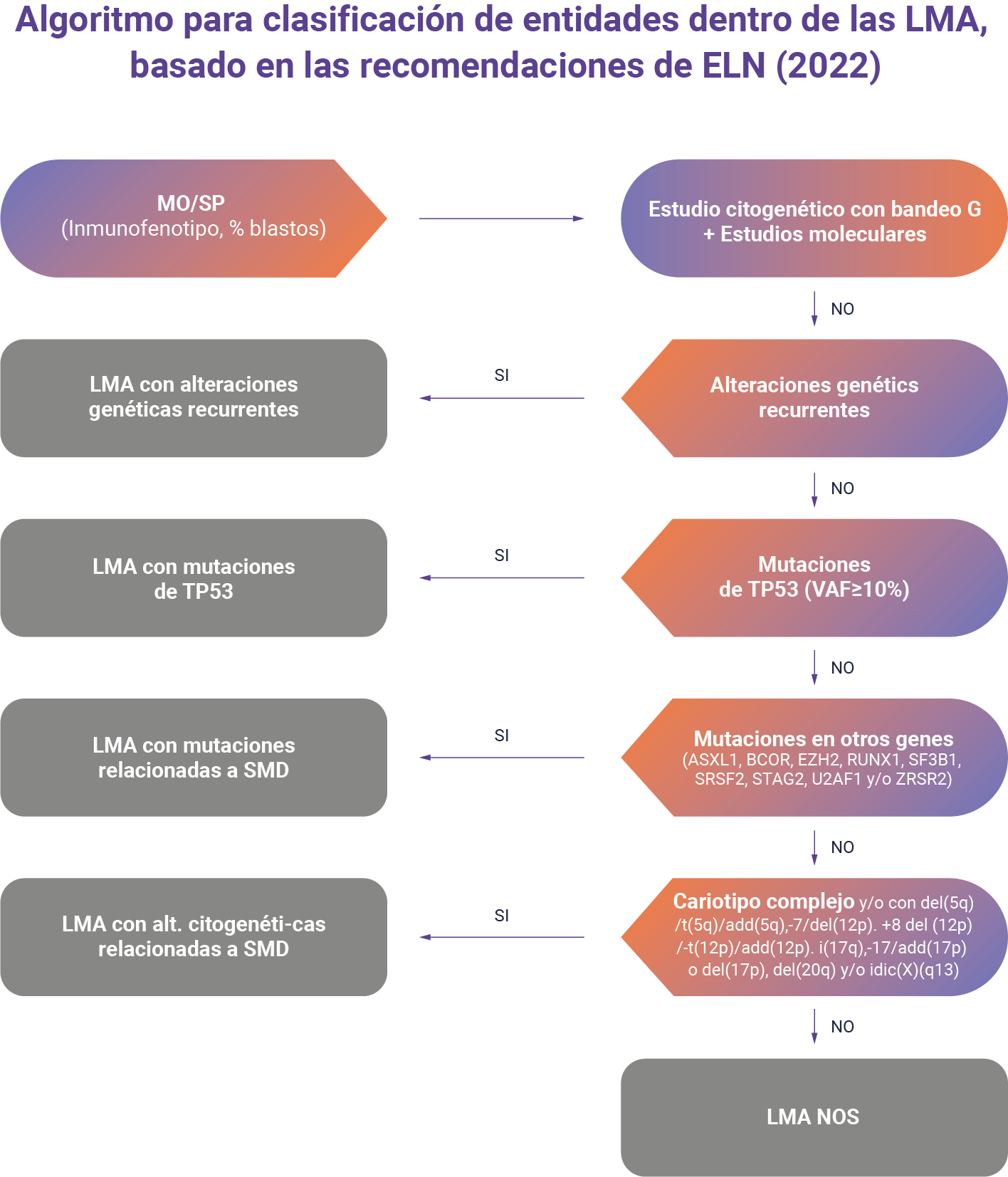
El diagnóstico de la LMA se basa en la medición de la morfología, el inmunofenotipado y la caracterización de la citogenética y la genética molecular de las células leucémicas.
- Anamnesis y exploración física.
- Laboratorio:
- Hemograma completo.
- Bioquimica sanguínea: hepatograma, ionograma, calcio, fosfor, ácido úrico, función renal, LDH. Proteinograma electroforético y dosaje de Igs.
- Pruebas de coagulación: coagulograma basal, fibrinógeno, D-dímeros o productos de degradación del fibrinógeno (PDF).
- Radiografía de tórax o TAC.
- Ecografía abdominal o TAC.
- Pan TAC (SPN, tórax, abdomen y pelvis) si hay organomegalias o sospecha de infección.
- RNM o TC cerebral si hay síntomas neurológicos.
- PET-TC en caso de sospecha de manifestación extramedular.
- Electrocardiograma, ecocardiograma y ecodoppler cardiaco.
- Evaluación cardiológica si hay antecedentes.
- Prueba funcional respiratoria, si hay antecedentes.
- Serologías virales.
- Grupo sanguínea ABO y Rh y estudio inmunohematológico.
- Test de embarazo para mujeres en edad fértil con consulta a ginecología y criopreservación de esperma en hombres.
- Evaluación odontológica y psicológica.
- Aspirado y/o biopsia de medula ósea:
- Morfología. Tinción May Grunwald-Giemsa. En MO contar 500 células y en SP 200 células.
- Citoquimica: mieloperoxidasa (MPO), estearasa especifica granulocítica (CIAE), estearasas no especificas para el linaje monocitico (ANAE). Criterio de positividad MPO: 3% de los blastos.
- Inmunofenotipo por citometría de flujo (Criterios de Euroflow). (Ver apartado)
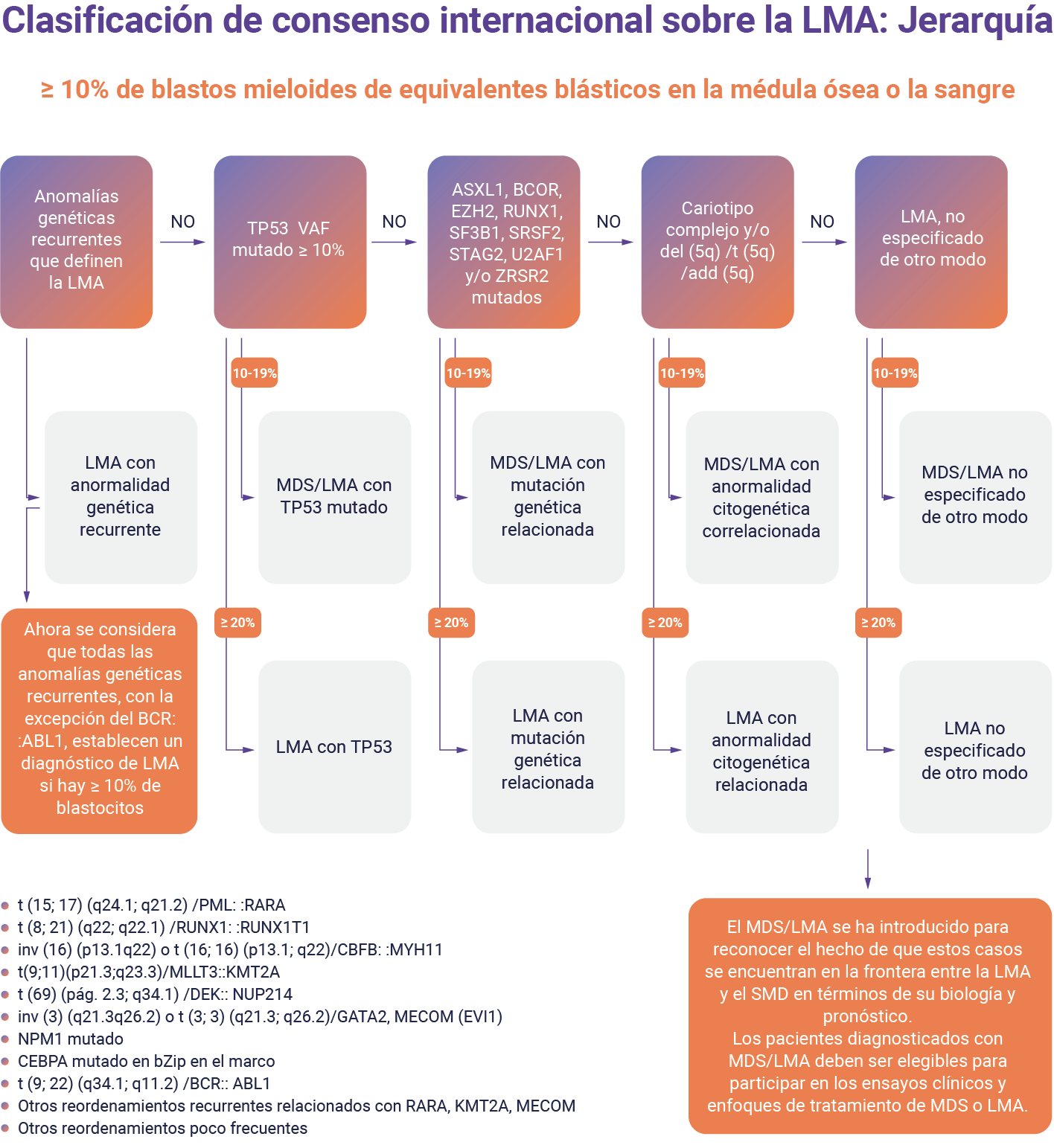
- Citogenética (cariotipo simple y bandeo G): es fundamental en la evaluación inicial. Deben analizarse como mínimo 20 metafases. En algunos casos la presentación clínica y el inmunofenotipo son orientativos del subtipo genético. Realizar en medula ósea, puede hacerse en sangre periférica en algunos casos.
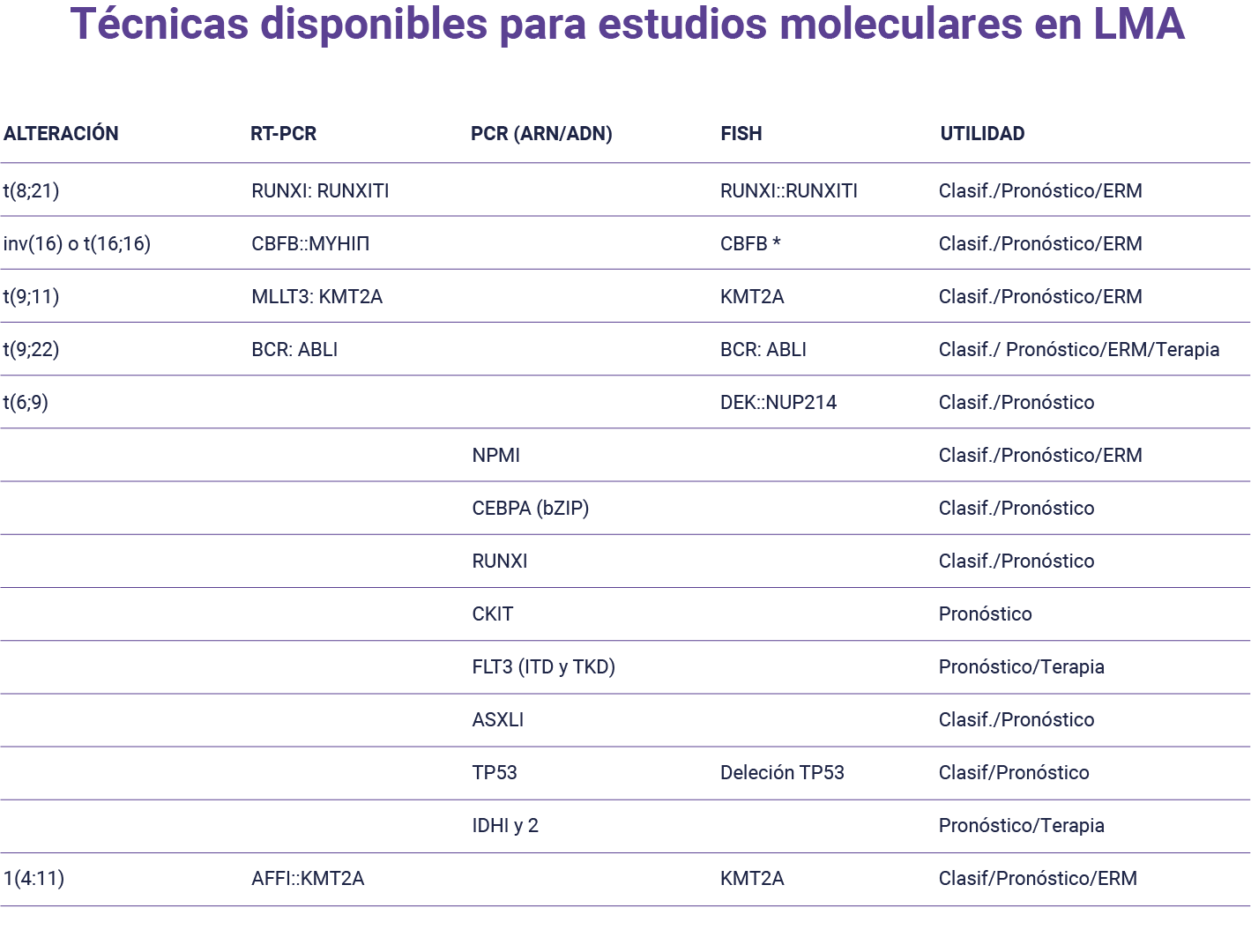
- Detección de alteraciones genéticas por FISH, RT-PCR: útiles para evidenciar alteraciones cripticas. Ante la sospecha clínica, inmofenotipica y/o morfológica compatible con leucemia promielocitica aguda (LPA), se recomienda búsqueda del rearreglo PML:RARA por FISH o RT-PCR o rearreglos del gen RARA por FISH (LPA no se tratará en este material). Se recomienda solicitar por FISH core binding factor (CBF) mediante sondas para detectar la t(8:21) e inv16.
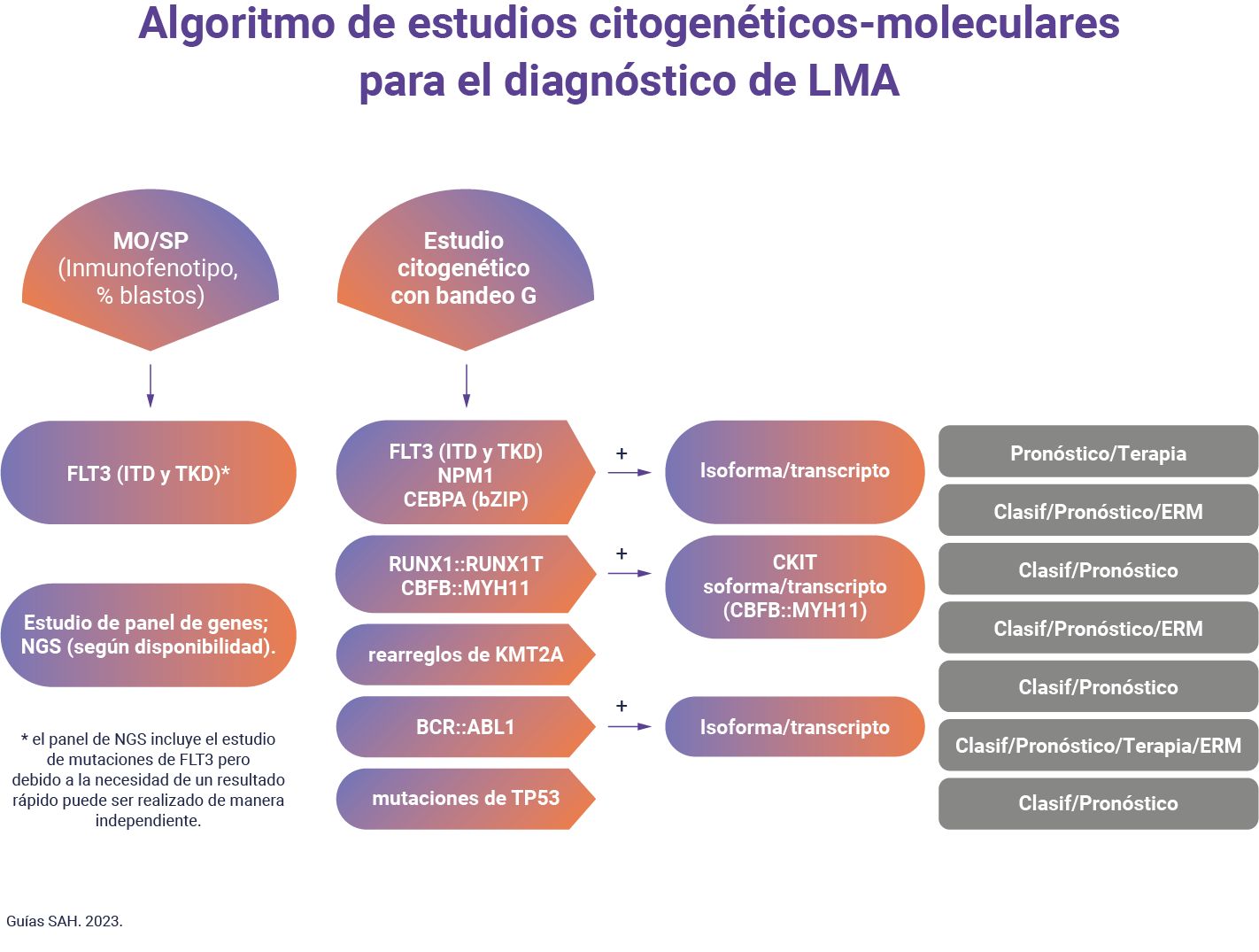
- Biología molecular: búsqueda de FLT3, NPM1 y CEBP alfa según los siguientes criterios:
- FLT3-ITD y TDK: en todos los pacientes. Para FLT3-ITD cuantificar ratio entre alelo mutado y no mutado (carga mutacional).
- NPM1: en todos los pacientes.
- CEBPa: en pacientes con cariotipo normal, si bien se recomienda en todos los pacientes.
- Estudio de HLA a paciente y familiares (si se considera posibilidad de trasplante de medula ósea).
Franziska W. Pathophysiology of acute myeloid leukemia. Acta Haehematológica. 2024. Sanz M y Carreras E. Manual práctica de hematología clínica. Sexta edición. 2022. Guía SAH. 2023
Consideraciones especiales
Inmunofenotipo por citometría de flujo: es fundamental para determinar las líneas celulares involucradas en el clon leucémico e identificación de patrones de expresión antigénica anómalos o aberrantes. Estos datos son de utilidad para cuantificar luego la enfermedad residual medible (ERM).
Perfil genético-molecular:
es fundamental dado que proporciona información para categorizar el riesgo/pronostico, definir el tipo de tratamiento, evaluación de la respuesta al tratamiento.
Determinacion del perfil genético completo:
solo es posible por técnicas de secuenciación tales como NGS, que permiten estudiar múltiples alteraciones y rearreglos génicos en forma simultánea. No obstante, ante la urgencia del diagnostico y de no contar con esta posibilidad en forma rápida, se sugiere el screening de algunas alteraciones moleculares por PCR convencional como por ejemplo FLT3 (ITD y TKD). En ese caso preservar muestra del diagnóstico, pre tratamiento< para estudio posterior por NGS
AR-VEN-250029