MIGRAÑA
Tratamiento Agudo
Objetivo: rápido y completo alivio
- Sin recurrencia dentro de las siguientes 24 hrs
- Sin efectos secundarios
- Recuperar la funcionalidad del paciente
Reglas
- Usar la medicación al inicio del episodio, dolor leve
- Ruta apropiada de administración
- Co-administración de procinéticos o antiémeticos
Declaración de consenso de la American Headache Society sobre la integración de nuevos tratamientos en la práctica clínica
- Ataques leves-moderados1
- Utilizar AINE, analgésicos no opiáceos, paracetamol o combinaciones de analgésicos con cafeína.
- Ataques moderados-graves ( o ataques leves-moderados que responden mal a la terapia inespecífica).1
- Utilizar agentes específicos para la migraña (triptanes, dihidroergotamina), antagonistas de molécula pequeña del receptor CGRP (gepantes), agonistas selectivos de los receptores de serotonina (5-HT1F) (titanes).
- Criterios para iniciar gepantes, ditanes o dispositivos neuromoduladores para el tratamiento agudo1
- Prescrito por un médico autorizado, paciente >18 años de edad con diagnóstico de migraña (con o sin aura) o migraña crónica.
- Contraindicación o capacidad a para tolerar triptanes o respuesta inadecuada a dos o más triptanes orales, evaluada mediante un cuestionario validado de resultados reportados por el paciente en tratamiento agudo o un certificado médico.
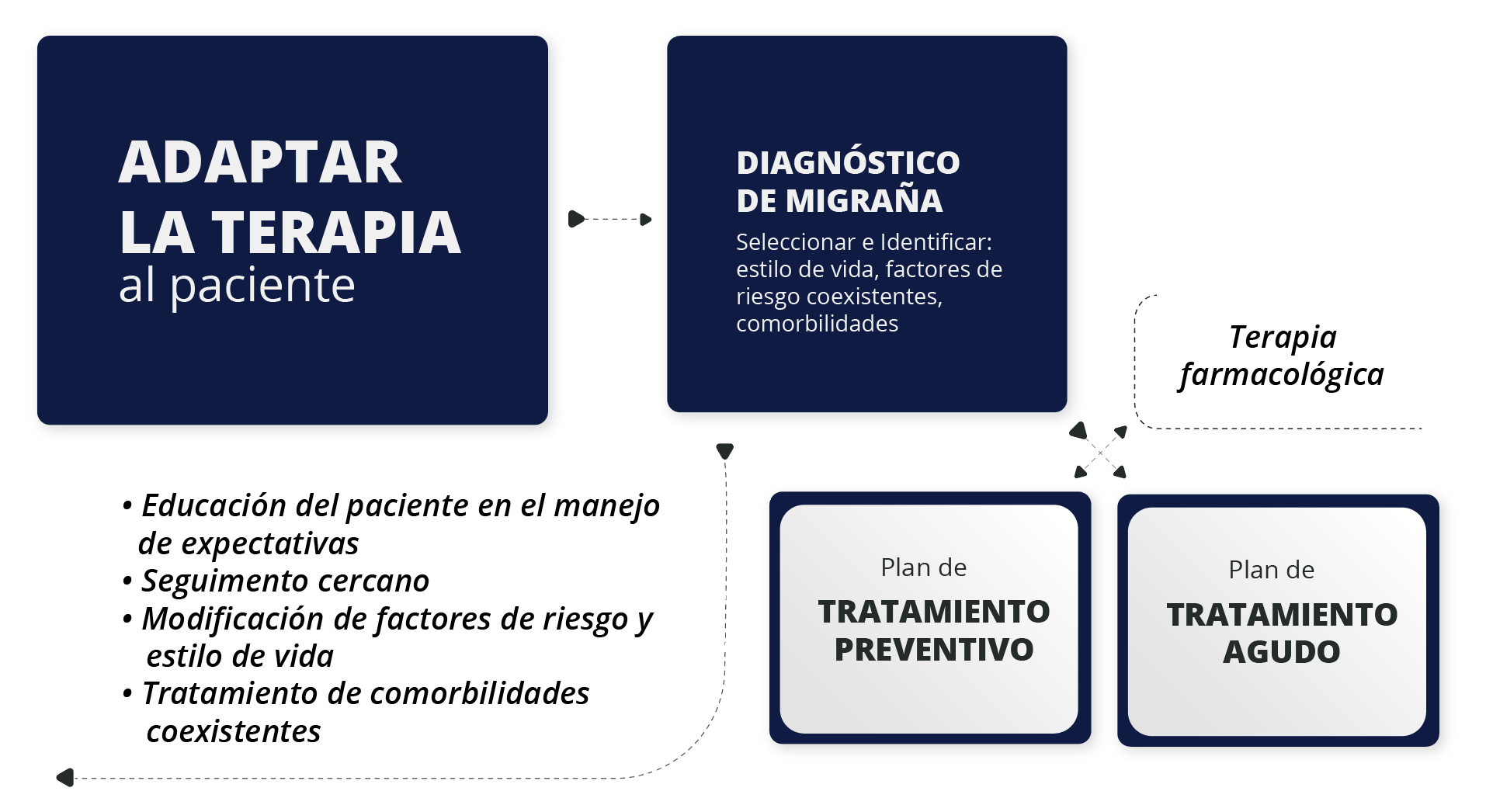
Tratamiento Preventivo
En quienes indicar tratamiento preventivo
- 4 o + ataques/mes o >2 días/ semana
- Episodios recurrentes que interfieren con la calidad de vida
- Fallo o contraindicación tratamiento agudo
- Crisis incapacitantes/ Emergencia
- Crisis prolongas
- Migraña Crónica
- Migraña con Aura prolongada, con aura de tronco, infarto migrañosa
Continuum (Minneap Minn) 2015; 21(4):973-989
Objetivos del preventivo
- Disminuir 50 % frecuencia de los ataques
- Disminuir intensidad y duración
- Mejorar la respuesta al tratamiento agudo
- Prevenir la progresión a la cronicidad
- Disminuir el compromiso de calidad de vida
40 % de los pacientes con migraña reúnen criterios para tratamiento preventivo
Antonaci et al. SpringerPlus (22016)5;637; Silberstein SD, AHS, Neurology 78(17):1337-1345
Preventivos via oral
Tabla 1. Fármacos para uso como tratamiento, preventivo, en la migraña
Tipo tratamiento preventivo | Compuesto | Dosis |
| β-bloqueantes | Propranolol | 40-160 mg |
| Nadolo | 40-160 mg | |
| Aenool | 50-200 mg | |
| Neuromoduladores | Topiramato | 50-200 mg |
| Valproato | 300-1.500 mg | |
| IECA/ARA-II | Lisinopril | 5-20 mg |
| Candesartán | 8-32 mg | |
| Antagonistas del calcio | Flunarizina | 2,5-10 mg |
| Antidepresivos | Amitriptilina | 10-75 mg |
| Venlafaxina | 75-100 mg |
Tabla 2. Efectos adversos de los principales fármacos útiles en el tratamiento preventivo de la migraña
Efectos frecuente | Efectos raros | |
| Beta bloqueadores | Fatiga Mareo Náuseas Hipotensión ortostática lmpotencia Insomnio/pesadillas Frialdad distal | Depresión Bradicardia sintomática Insuficiencia cardíaca Bronco constricción |
| Topiramato | Parestesia distales Síntomas cognitivos Trastornos intestinales Pérdida de peso | Glaucoma Litiasis renal Depresión |
| Ácido valproico | Náuseas/vómitos Somnolencia Sobrepeso Temblor Alopecia | Hepatotoxicidad Quistes ováricos Trombocitopenia |
| Flunarizina | Depresión Somnolencia Sobrepeso | Parkinsonismo Galactorrea |
| Amitriptilina | Somnolencia Estreñimiento Sobrepeso Sequeda de piel/mucosas Palpitaciones | Síntomas cognitivos Retención urinaria Glaucoma |
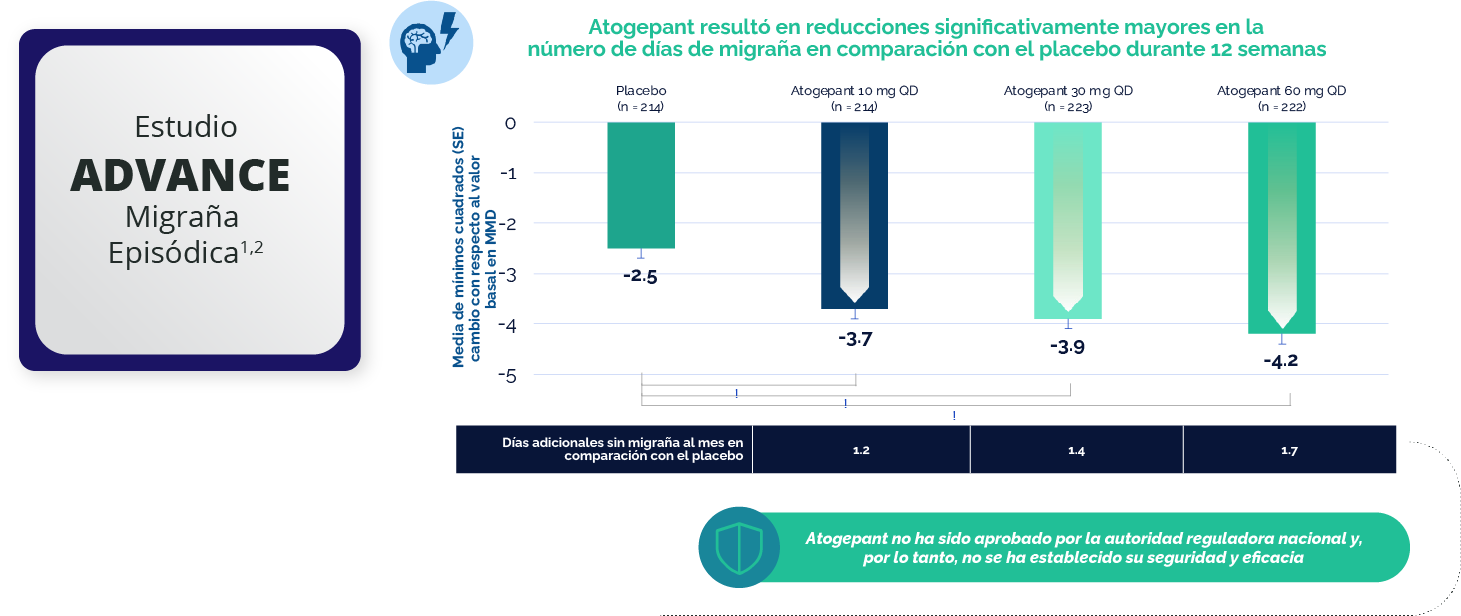
ATOGEPANT REDUCCIÓN DE LOS DÍAS DE MIGRAÑA AL MES
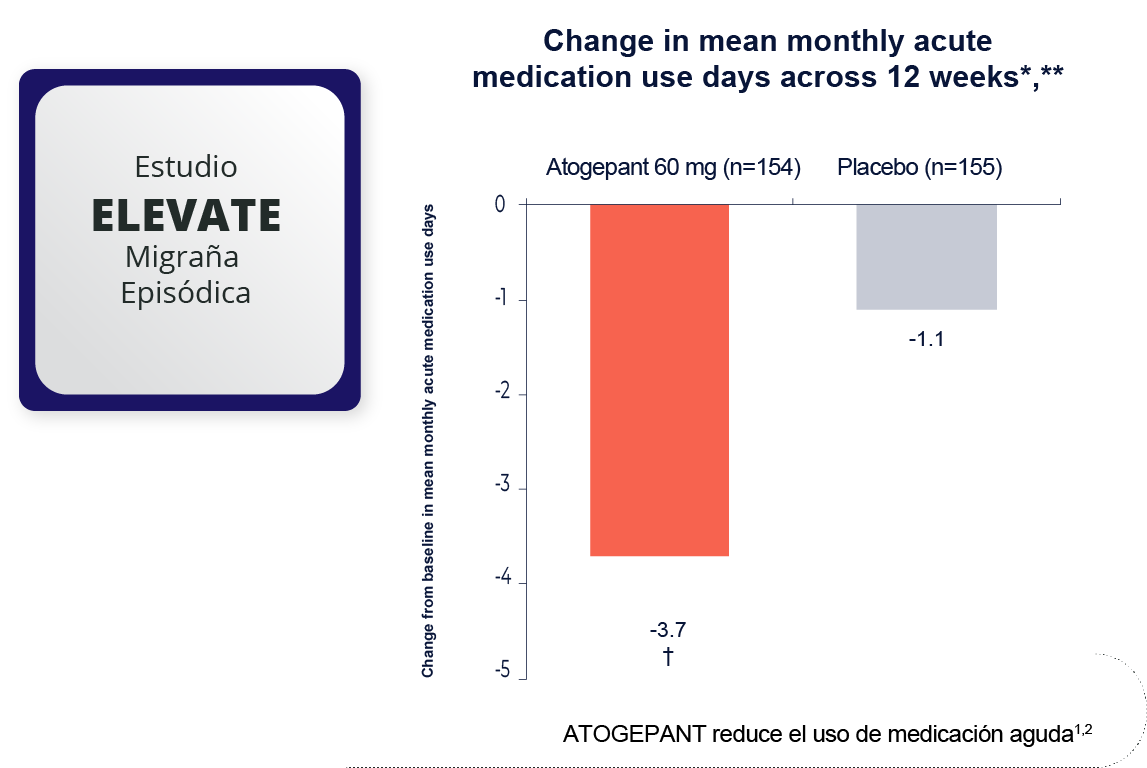
*Incluye a todos los participantes asignados aleatoriamente que recibieron ≥ 1 dosis de atogepant o placebo, que tuvieron un período basal con datos del diario electrónico evaluables y al menos un período posterior al basal de 4 semanas (Semanas 1–4, 5–8 o 9–12) con datos del diario electrónico evaluables durante el período de tratamiento doble ciego; †Indica una diferencia estadísticamente significativa versus placebo; valor p ajustado < 0.001.
LS= mínimos cuadrados; mITT= intención de tratar modificada; MMD= días de migraña mensuales; QD= una vez al día; SE = error estándar.
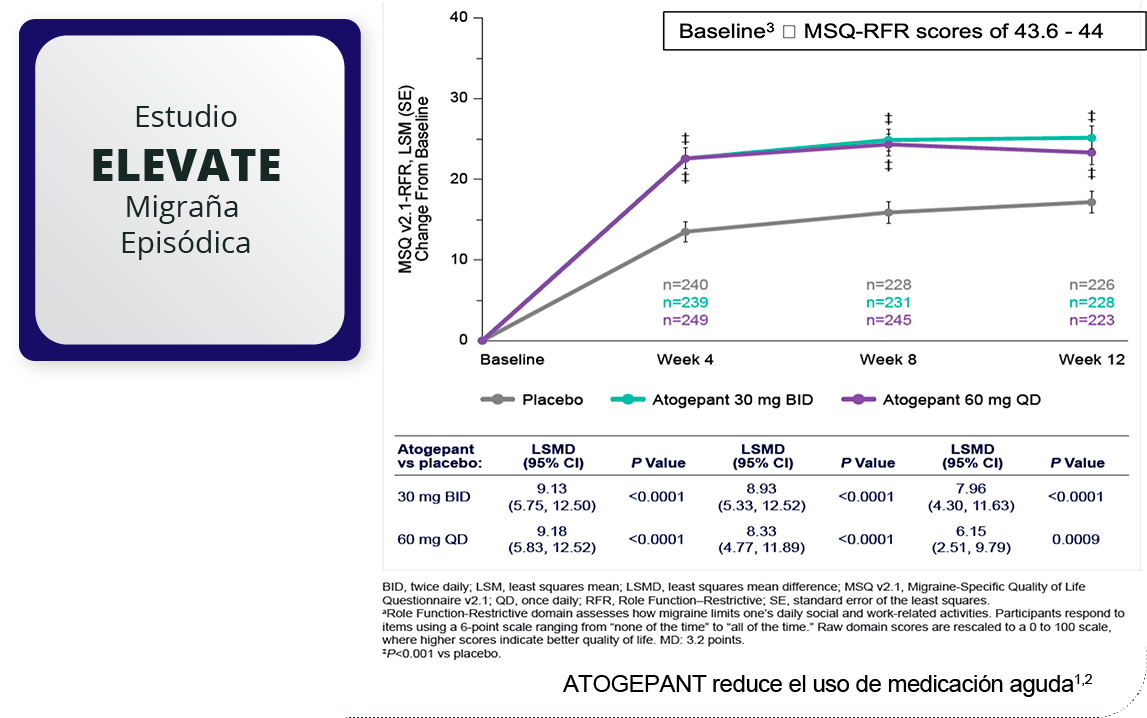
La dosis de 30 mg de atogepant se ha estudiado en los estudios Fase III. La dosis de 30 mg no está autorizada en Europa.
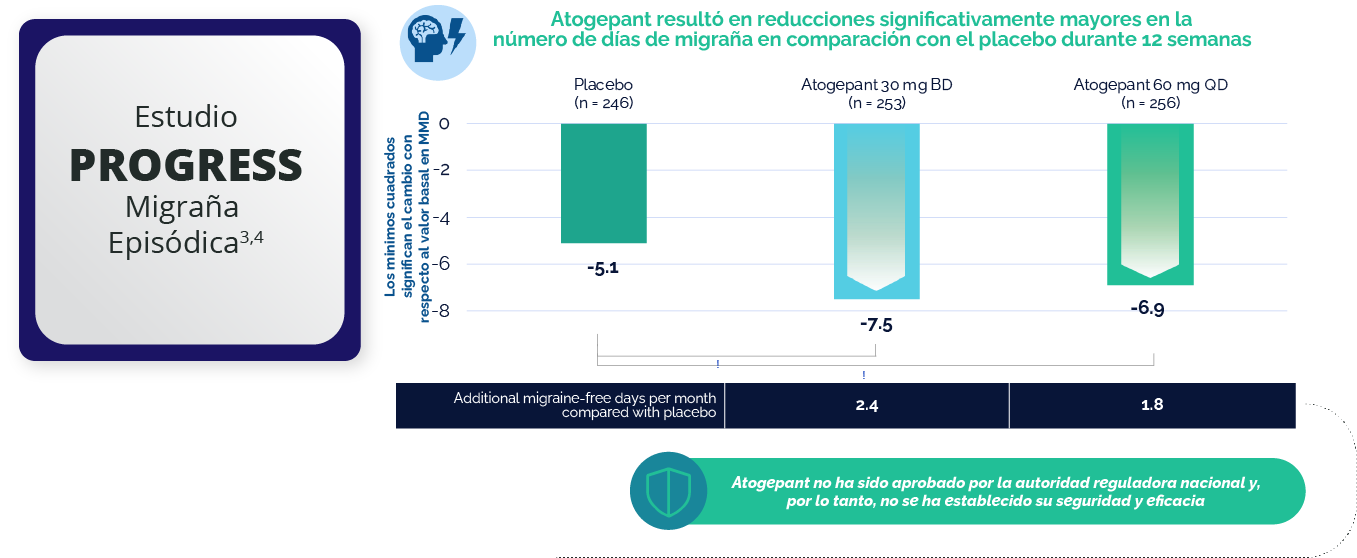
Población mITT Promedio basal (DE) de días de migraña mensuales (por diario electrónico): placebo 19.0 (4.8); atogepant 30 mg BID 18.6 (5.1); atogepant 60 mg QD 19.2 (5.3).
*Indica una diferencia media de mínimos cuadrados estadísticamente significativa vs placebo; p<0.0001 atogepant 30 mg BID; p=0.0009 atogepant 60 mg QD. Los valores p se ajustaron por comparaciones múltiples. Las barras de error representan el error estándar.
BID= dos veces al día; LS= mínimos cuadrados; mITT= intención de tratar modificada; MMD= día de migraña mensual; SD=desviación estándar; QD= una vez al día.
La dosis de 30 mg de atogepant se ha estudiado en los ensayos de Fase III. La dosis de 30 mg no está autorizada en Europa.
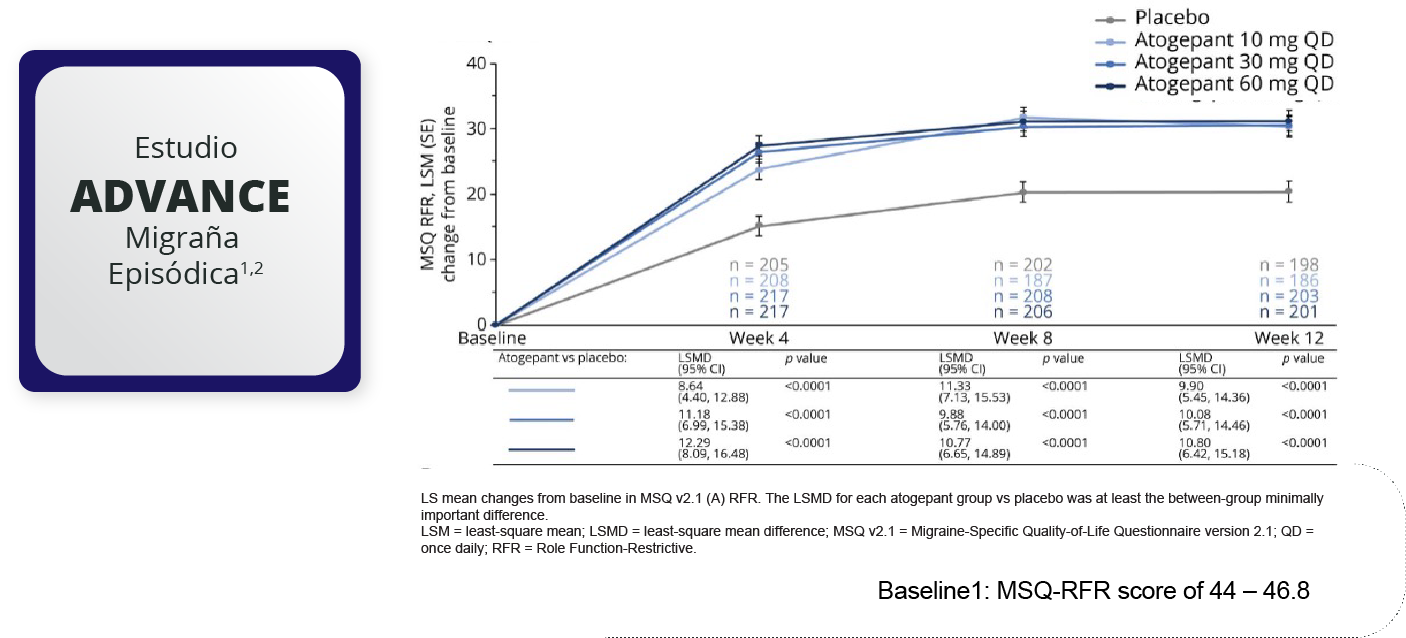
1. Ailani J, et al; ADVANCE Study Group. Atogepant for the Preventive Treatment of Migraine. N Engl J Med. 2021 Aug 19;385(8):695-706 2. Ailani et al. Atogepant Significantly Reduces Mean Monthly Migraine Days in the Phase 3 Trial (ADVANCE) for the Prevention of Migraine. Poster presented at the International Headache Congress, September 8-12, 2021 3. Pozo-Rosich P et al. Atogepant for the Preventive Treatment of Chronic Migraine: Results From the PROGRESS Phase 3 Trial. Presented at: American Headache Society (AHS); June 9-12, 2022; Denver, CO, USA 4. Pozo-Rosich P, et al. Atogepant for the preventive treatment of chronic migraine (PROGRESS): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2023 Sep 2;402(10404):775-785.
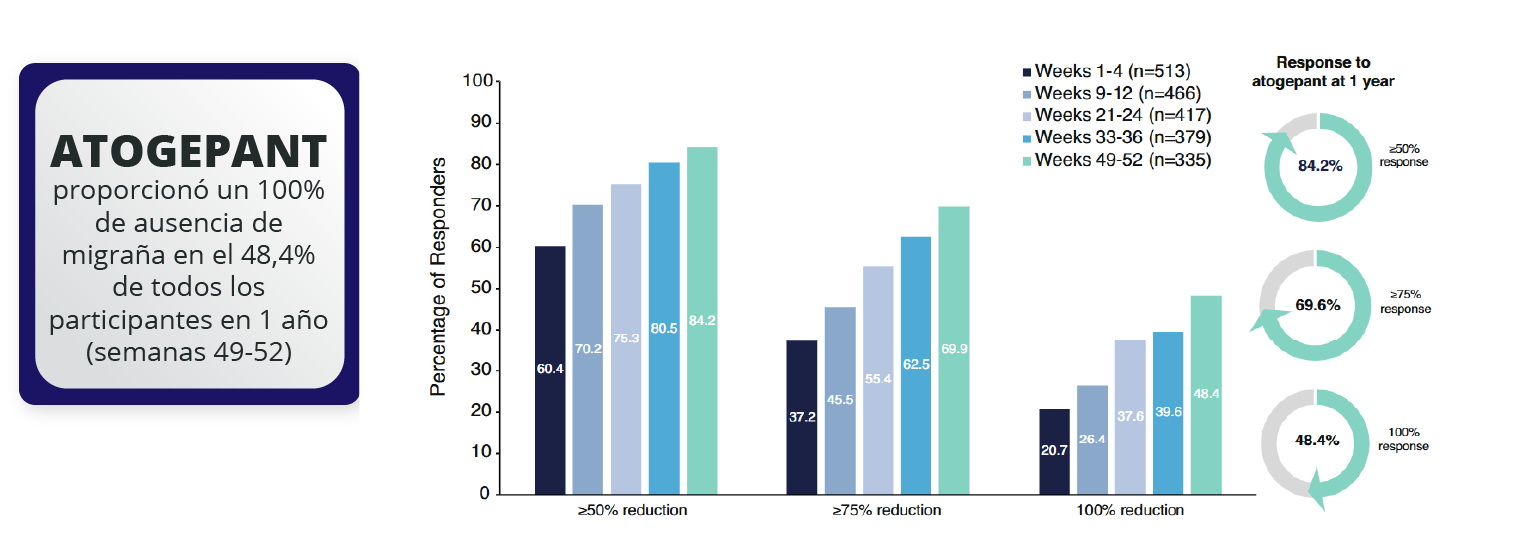
Estudio 302 Ensayo de seguridad a largo plazo para pacientes con migraña episódica
Tabla 3. Resultados de seguridad y tolerabilidad
Category,* n (%) | Atogepant 60 mg (n=543) |
| TEAE | 364 (67.0) |
| Relacionado con el tratamiento TEAE | 98 (18.0) |
| Muerte** | 2 (0.4) |
| TEAEs serios | 24 (4.4) |
| TEAE que conduce a la interrupción | 31 (5.7) |
*Los participantes se contaron solo una vez dentro de cada categoría. | |
En el grupo Atogepant, la mayoría de los AAET fueron leves (25,8%, 140/543) o moderados (34,4%, 187/543)
AAE que dieron lugar a la interrupción del tratamiento para los pacientes tratados con Atogepant:
- Náuseas (3/543, 0.6%)
- Fatiga (2/543, 0.4%)
- Mareos (2/543, 0.4%)
- Erupción cutánea (2/543, 0.4%)
Los TEAEs más comúnmente reportados en el grupo Atogepant fueron:
- Infección del tracto respiratorio superior (56/543, 10,3%)
- Estreñimiento (39/543, 7.2%)
- Náuseas (34/543, 6.3%)
- Infección del tracto urinario (28/543, 5,2%)
Seguridad migraña crónica
Tabla 5. TEAEs notificados en la población de seguridad* del ensayo PROGRESS
Category, n (%) | Atogepant 60 mg | Placebo |
Placebo | 165 (63) | 126 (49) |
| Los siete principales TEAE reportados en el ≥2% de los participantes en cualquier grupo | ||
| Constipación | 26 (10) | 8 (3) |
| Náuseas | 25 (10) | 9 (4) |
| Mareos | 12 (5) | 8 (3) |
| Nasofaringitis | 11 (4) | 11 (4) |
| Disminución del apetito | 9 (3) | 0 (0) |
| Fatiga | 8 (3) | 7 (3) |
| Pirexia | 8 (3) | 3 (1) |
| TEAE relacionados con el tratamiento | 45 (17) | 34 (13) |
| TESAEs | 7 (3) | 3 (1) |
| TEAEs que conducen a interrupciones | 9 (3) | 10 (4) |
Ninguno de los TESAE fue considerado relacionado con el fármaco en estudio por el investigador. | ||
ABBV-AR-00235-MC